转自:药时空
EGFR、HER3虽是研究已久的老靶点,但抗体、ADC等大分子药物的开发却多有坎坷。HER3尚未有靶向药物获批,EGFR抗体在NSCLC获批有两款抗体,但也仅Amivantamab双抗撑得起门面。下文通过回顾对比早期临床项目,看看两个经典靶点与ADC结合之下的BL-B01D1有何特别之处?
01
EGFR ADC
艾伯维开发Depatuxizumab Mafodotin(ABT-414)由EGFR抗体ABT-806、单甲基澳瑞他汀-F(MMAF)毒素,通过不可裂解的马来酰亚胺己基连接子偶联,DAR值为4。艾伯维强调了ABT-806抗体,对比西妥昔单抗与panitumumab对EGFR亲和力较弱,降低了对正常组织的副作用。
ABT-414以胶质母细胞瘤(GBM)为主要开发方向,在I期临床中显示出治疗潜力,也同时发现存在较高的眼毒性(91%)。最终ABT-414在新发GBMIII期以及复发GBM II期两项临床中,主要终点OS与对照组间没有显著性差异。ABT-414曾在1/2 期临床中探索在鳞状NSCLC等实体瘤的治疗潜力,但是并未继续推进。
艾伯维第二款EGFR ADC ABBV-221,由AM1抗体与单甲基奥瑞他汀-E(MMAE)毒素组成,DAR值为3。ABBV-221提高了抗体部分对EGFR的亲和力,AM1比AT806亲和力提高10倍,不过仍保持低于西妥昔单抗,三者KD值分别为2.2E-07M、2.3E-06M、4.0E-9M。
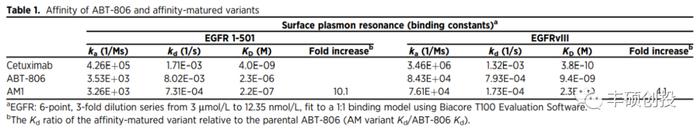
图1 AM1、AT806、西妥昔单抗结合EGFR亲和力数据(来源:资料1)
临床前研究显示,亲和力提高以及Kd降低,让ABBV-221在肿瘤摄取上要优于ABT-414。同时,抗体部分亲和力提高(非更换MMAE毒素),也增强了ABBV-221体内抗肿瘤活性。为降低眼毒性,也将MMAF毒素换为MMAE。不过ABBV-221在I期临床后便终止开发,原因为疗效与安全性不及预期。
Forbius公司的AVID100由高亲和力抗体MAB100,通过可剪切连接子与微管抑制剂 DM1偶联。MAB100结合EGFR的KD值为2 nM(和西妥昔单抗在一个数量级),采用了能够阻断EGFR功能的抗体,在临床前研究中有效降低了眼部不良反应。RP2D约为6 mg/kg Q3W(实体瘤),Forbius称是已报道的美登素类payload ADC中最高RP2D,不过这款产品在II期临床阶段终止。
乐普生物MRG003,为高亲和力人源化EGFR抗体(亲和力比西妥昔单抗提高约6至7倍),换为可降解的vc接头连接MMAE毒素。在已上市ADC药物中,Polivy、Padcev、Tivdak、维迪西妥均采用了vc-MMAE组合,相比当下热门的拓扑异构酶I抑制剂容易引发ILD,MMAE在这方面占有优势。MRG003 I期临床中表现出良好的安全性,大部分AEs程度较轻,≥3级TRAE主要为血液毒性,EGFR相关皮肤AE发生率也比西妥昔单抗、帕尼单抗报道的更低。
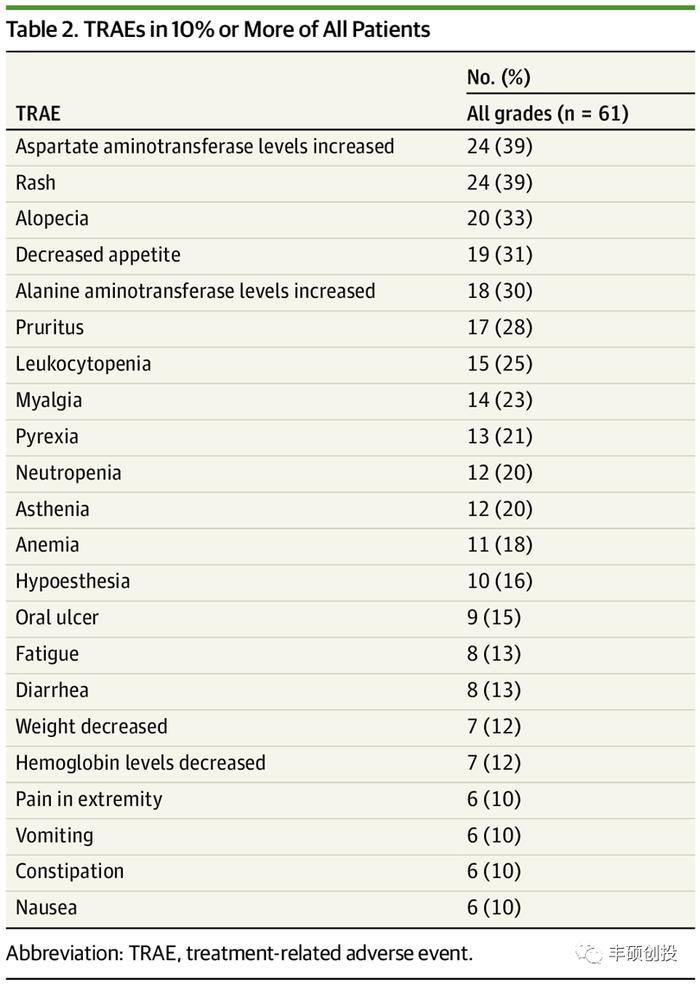
图2 MRG003晚期实体瘤I期临床中≥10%TRAE(来源:资料2)
小结:艾伯维在两款ADC的抗体筛选过程中,强调了ADC抗体部分的亲和力比已上市EGFR单抗要低,防止EGFR相关AE过高,最终却未能有所收获。而乐普MG003选用高亲和力抗体结合成熟的vc-MMAE平台,反也有不错的安全性表现,包括已上市的Akalux(Cetuximab sarotalocan),抗体部分也是直接用了西妥昔单抗。
02
EGFR双抗ADC
双抗或双抗ADC药物的开发的根本目的在于增效、减毒,期望通过多通路作用增强疗效,以及提高对肿瘤靶向性减低外周副作用。针对像正常组织也有表达的EGFR靶点,双靶药物能够实现降低外周在靶毒性更为重要。
德国Merk对EGFR/MUC1 ADC的介绍中,强调了通过双靶点定位提高特异性降低副作用,同时协同结合增加肿瘤内化率增强毒素作用的设计思路。
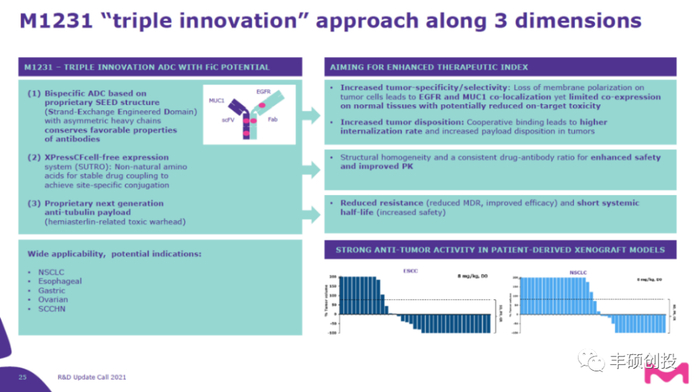
图3 德国默克EGFR/MUC1 ADC(来源:公开资料)
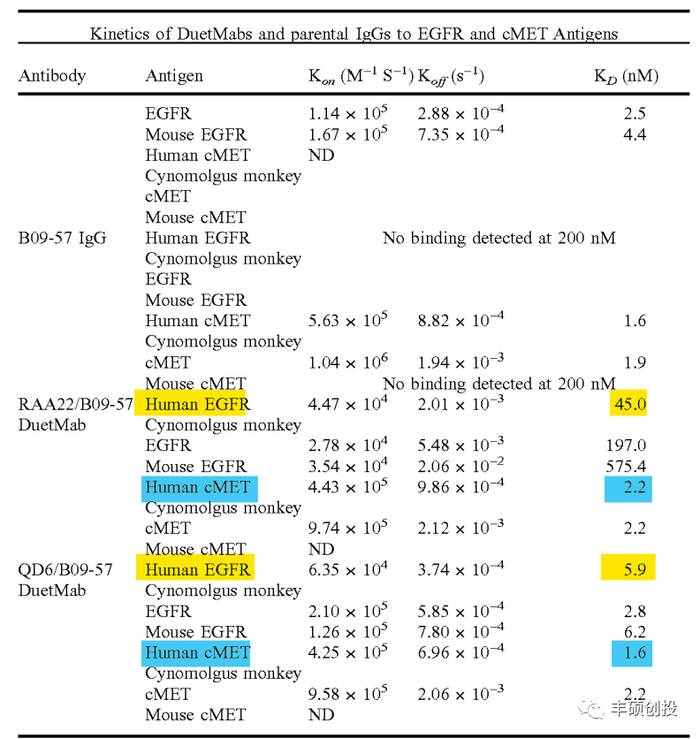
阿斯利康的EGFR/cMet双抗ADCAZD9592,通过可切割Linker将抗体与TOP1i载荷AZ14170132偶联,相较于EGFR,AZD9592对cMet具有更高的亲和力(>15 倍)。根据阿斯利康的专利,在与同一cMet臂B0957组合的双抗中,EGFR臂为高亲和力的DQ6(KD=5.9 nM)是,EGFR臂是内化作用的主要驱动;EGFR臂换为亲和力较低的RAA22(KD=45 nM)时,需要EGFR与c-Met臂共同参与才能有效内化(原文如下)。
另外两个可参考的双抗的案例为罗氏的EGFR/HER3双抗duligotuzumab,强生的EGFR/c-Met双抗amivantamab。
Duligotuzumab主要通过亲和力筛选获得Fab,双抗对HER3的选择性稍高于EGFR,亲和力Kd值分别为0.4 nM、1.9nM(比值为4.75倍),体外活性优于单独使用西妥昔单抗或HER3单抗。在II期临床中联用FOLFIRI治疗晚期CRC,duligotuzumab未能优于西妥昔单抗,因为早期胃肠道毒性等AE过高,患者过早地减少了化疗药物剂量导致ORR下降。
相对比duligotuzumab,amivantamab的筛选过程则更为严谨,亲和力检测,联同体外实验如EGFR磷酸化、MET磷酸化、癌细胞增值抑制的多层筛选才确定的。Amivantamab对MET结合亲和力是EGFR的35倍,KD值分别为0.04nM、1.4nM。Amivantamab已获批EGFR20ins NSCLC二线治疗,整体安全性可接受,EGFR相关AE主要为1-2级。
阿斯利康的专利提示,EGFR双抗筛选过程中对不同靶点亲和力的选择与平衡。在上文几款(候选)药物中,双抗对EGFR的选择都弱于另一靶点。结合早期艾伯维两款EGFR ADC的开发思路,这样设计的好处是,适当地降低对EGFR亲和力进而减少靶点相关AE,再提升对另一个靶点亲和力加强肿瘤特异性。
百利天恒子公司公开的EGFR/HER3双抗专利US2022075445(根据公司招股书,这个专利应该是双抗SI-B001,即BL-B01D1 ADC的抗体部分的说明)中,双抗对EGFR选择性比HER3更高,KD值相差1~2个数量级,思路基本和上述相反。
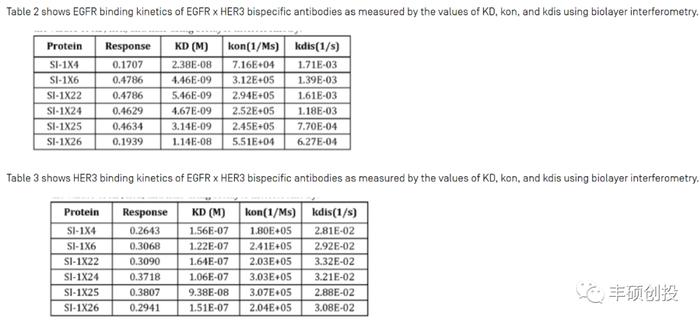
图5 百利天恒EGFR/HER3双抗亲和力数据(来源:资料4)
BL-B01D1在晚期实体瘤(NSCLC\NPC\HNSCC\SCLC)临床研究中具有可接受的安全性,≥3级TRAE主要为血液毒性,EGFR相关AE发生率较低均为1-2级,如皮疹13%、腹泻17%、恶心33%。对比在不同患者人群中EGFR/HER3双抗的副作用,duligotuzumab在治疗晚期CRC中皮疹、腹泻、恶心发生率为79%、91%、49%。

图6 BL-B01D1在晚期实体瘤中的安全性(来源:公开资料)
目前看来,BL-B01D1的确一定程度上EGFR相关AE,也许双靶点中对EGFR选择性高的思路也是可行?这里也对应了上文中提到的MRG003和Cetuximab sarotalocan的设计。
03
HER3 ADC
第一三共的HER3 ADC(U3-1402,HER3-DXd)由patritumab抗体通过可裂解的四肽连接子与DXd偶联,DAR值为8。2023JSMO上公布的最新数据显示,在既往接受EGFR-TKI±PBC治疗失败的EGFR突变NSCLC,cORR=40%,DCR=78.4%,mDOR=7.6个月,mPFS=6.4个月,mOS=15.8个月。
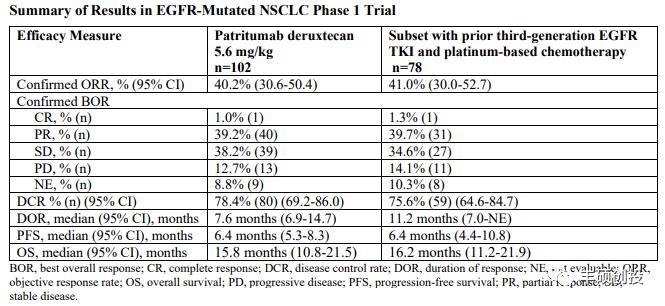
图7 U3-1402在TKI耐药NSCLC中疗效(来源:2023JSMO)
Patritumab其实也是一款在NSCLC III期临床中失败的HER3抗体,在第一三共通过DXd ADC平台的改造,重新点燃了HER3靶向治疗NSCLC的希望。
04
BL-B01D1
百利天恒BL-B01D1的产品设计整体看来是make sense的,包括双抗体部分对EGFR有更高的选择性,毒素也是应用成熟的喜树碱类payload技术。从目前临床数据看来,安全性没有太大问题EGFR相关AE发生率较低,而有关BL-B01D1的临床疗效的讨论比较多。
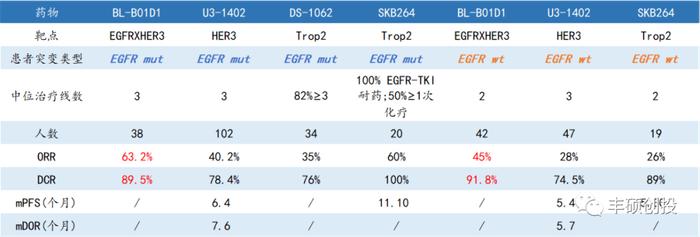
BL-B01D1在EGFRmut NSCLC患者中,早期公布的数据中ORR为87.5%(n=16),最新数据中却下降到63.2%(n=38)。在EGFRwtNSCLC人群中ORR为44.9%(n=49),比早期在15例患者中33%的ORR有所提升。推测是因为早期患者样本量较少,外加细分患者入组对数据造成较大影响,如EGFR不同突变类型,或伴有不同驱动基因等。
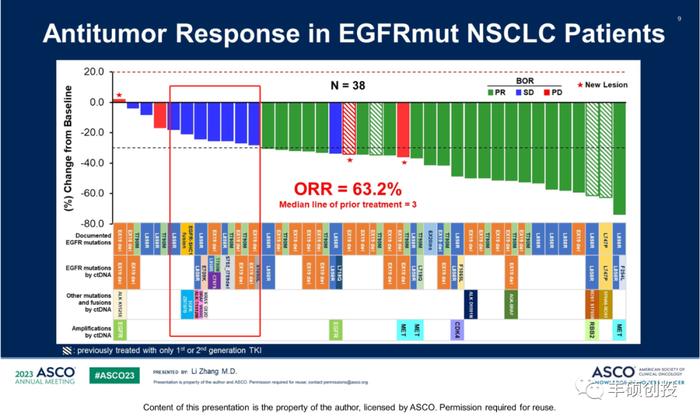
图8 BL-B01D1在EGFRmut NSCLC中疗效评价(来源:公开资料)
U3-1402也有相似的情况发生,在EGFRwt携带驱动基因(如KRAS\NRAS\ALK\ROS1等)的NSCLC患者中(NCT03260491),早期ORR为35%(n=17),最新数据中为28.6%(n=21)。
另外一个导致ORR下降的可能原因是,早期获得PR的患者出现新病灶复发(PD)的情况(如图中框出的*病例),因为目前BL-B01D1治疗后只有部分患者进行1次肿瘤评估,PR也包含了治疗中的患者,ORR数据还不算成熟,不比confirmend ORR有信服力。
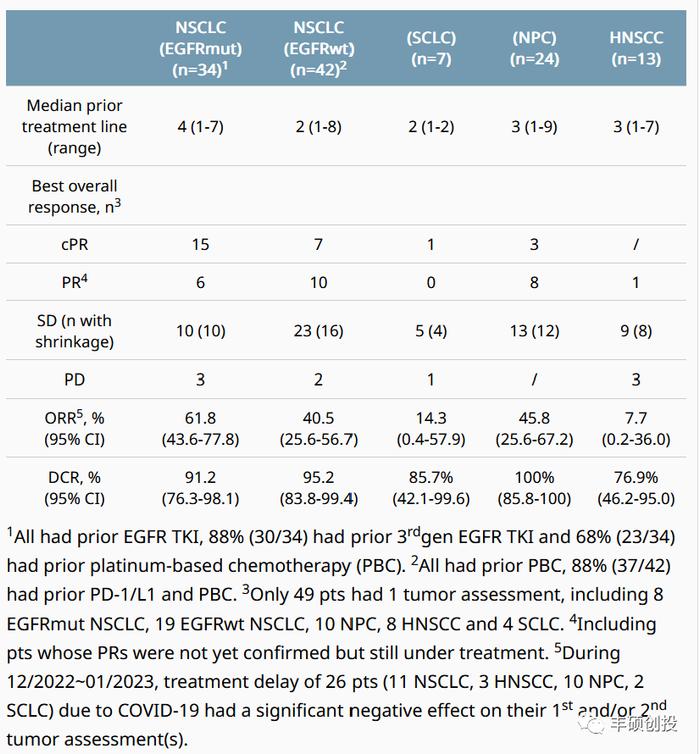
图9 BL-B01D1在晚期实体瘤中疗效评估(来源:资料5)
因此,我们应该审慎地看待早期小样本数据,BL-B01D1的疗效也需要更多的临床数据验证,在PFS、DOR数据公布后才好进一步说明。另外,EGFR突变、EGFR阴性NSCLC应当都是需要做III期对照临床上市,BL-B01D1要走的路还很长。
参考资料
1、Characterization of ABBV-221, a Tumor-Selective EGFR-Targeting Antibody Drug Conjugate
2、Characterization of ABBV-221, a Tumor-Selective EGFR-Targeting Antibody Drug Conjugate
3、https://patents.google.com/patent/US20230183358A1/en
4、WO2023028548 - BISPECIFIC TETRAVALENT ANTIBODY TARGETING EGFR AND HER3
5、BL-B01D1, a first-in-class EGFRxHER3 bispecific antibody-drug conjugate (ADC), in patients with locally advanced or metastatic solid tumor: Results from a first-in-human phase 1 study