(报告出品方/作者:东北证券,刘宇腾)
1.“魔法子弹”高效杀伤肿瘤,精准靶向治疗时代呼之欲出
1.1.抗体+连接子+毒素—抗体偶联药物(ADC)兼具靶向性、杀伤性
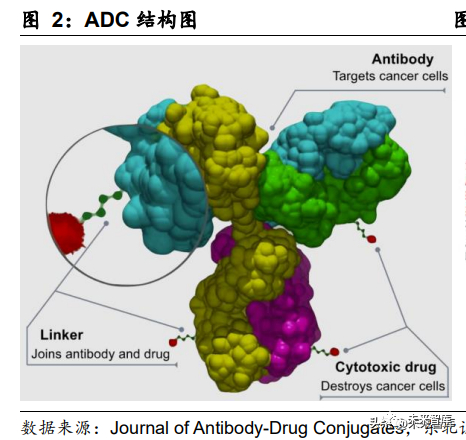
抗体偶联药物(antibody drug conjugate,ADC)最早起源于 1913 年,诺奖得主德 国科学家保罗·埃尔利希 Paul Ehrlich 首次提出“Magic bullets”(魔法子弹)设想:将细胞毒药物安装在特异性靶向肿瘤细胞的载体上,便可实现在不伤害正常细胞的 前提下精确杀死癌细胞。ADC 药物主要由三个部分组成:(1)单克隆抗体(antibody):负责有选择性地靶 向在肿瘤微环境中的肿瘤细胞;(2)连接子(linker):连接单克隆抗体和毒性物质 的连接符;(3)毒性物质(drug):杀死靶细胞的细胞毒性化疗有效载荷。
作为一种新型的肿瘤治疗方法,ADC 主要通过选择性地将强效化疗细胞毒素直接投 递到肿瘤细胞来发挥功能,此类新型靶向药物的理论基础区别于传统上单纯的靶向 联合化疗,以单克隆抗体作为化疗的载体,既能够实现 1+1>2 的抗肿瘤效应,又能 体现高效低毒的治疗优势。相比之下,传统的化疗无法将健康细胞从肿瘤细胞中区 分出来,而抗体药物偶联物具有独特的靶向能力,在经历三代技术迭代,现阶段抗 体偶联药物已经能够做到低毒性基础上定向杀死肿瘤细胞,同时旁观效应可以更大 程度上保证肿瘤临近细胞的清除,因此,抗体偶联药物正在成为肿瘤治疗领域的一 代新星。
ADC 药物主要作用机制为:ADC 药物进入体内后,抗体部分与表达肿瘤抗原的靶 细胞特异性结合,内化进入肿瘤细胞后,进入溶酶体进行降解,小分子细胞毒药物 在胞内以高效活性形式被足量释放,从而完成对肿瘤细胞的杀伤。
1.2.CDE频发指导意见规范ADC临床,为百亿赛道保驾护航
CDE 两月内连发 ADC 指导原则,指明开发方向规范技术要求。2022 年 7 月,CDE 发布“关于公开征求《抗体偶联药物非临床研究技术指导原则》意见的通知”,意在更 好指导和促进抗体偶联药物(ADC)的研究和开发。此指导原则分别就 ADC 的药 理学研究、药代动力学研究、毒理学研究、人体首次临床试验起始剂量拟定以及支 持临床试验和上市申请的分阶段非临床研究策略等内容进行了阐述,对 ADC 药物 非临床研究方向、重点研究内容作出了详细指导。该指导原则结束了国内 ADC 非 临床研究只能遵循 ICH 指导意见的历史。
同年 9 月,CDE 发布《抗肿瘤抗体偶联药物临床研发技术指导原则(征求意见稿)》。此指导原则重点对 ADC 药物临床开发的总体思路、差异化竞争、联合治疗设计等 作出指导,为国内企业研发提供 ADC 创新药物应遵循的总方向和出发点。两次指 导原则的发布,标志着国内 ADC 药物从非临床开发的技术重点到临床开发的总体 思路均有具体内容引领,将会进一步规范 ADC 领域,为 ADC 研发提供有效的引导 和支持。
1.3.ADC赛道交易不断,临床价值受国际认可
国际医药巨头 MNC 辉瑞收购 ADC 龙头企业,持续加码助推 ADC 赛道热度制高 点。2023 年 3 月 13 日,国际医药巨头 MNC 辉瑞宣布以总价约 430 亿美元价格现 金收购 Seagen。根据公司官网显示,被收购方 Seagen 2022 全年总营收 20 亿美 元,产品净销售额同比增长 23%至 17 亿美元,其中 3 款 ADC 药物分别贡献了 8.39 亿美元(+19%,Adcetris)、4.51 亿美元(+33%,Padcev)、0.63 亿美元(+923%, Tivdak)。
根据公司公告,2023 年 Seagen 预计总营收将达到 21.4-22.4 亿美元,产品净销售 额将达到 19.25-20 亿美元,同比增长 13%-17%,归功于 Adcetris、Padcev 的销 售。与此同时,Seagen 分别与两家国内创新 ADC 企业存在合作协议:(1)根据荣昌生物 2021 年 8 月 9 日《与 Seagen 订立许可协议》公告,荣昌生物 独家授权开发维迪西妥单抗(2 亿美元首付款+最多达 24 亿美元的里程碑付款+销 售分成);(2)2022 年 9 月 27 日,Seagen 独家授权 TIVDAK 开发与商业化给再鼎医药 (3000 万美元首付款+里程碑付款+销售分成)。2023 年 Seagen 研发费用将有所增加,达到 14.24-15.25 亿美元,进一步推进合作 开发商业化 ADC 产品的研发与创新进程。
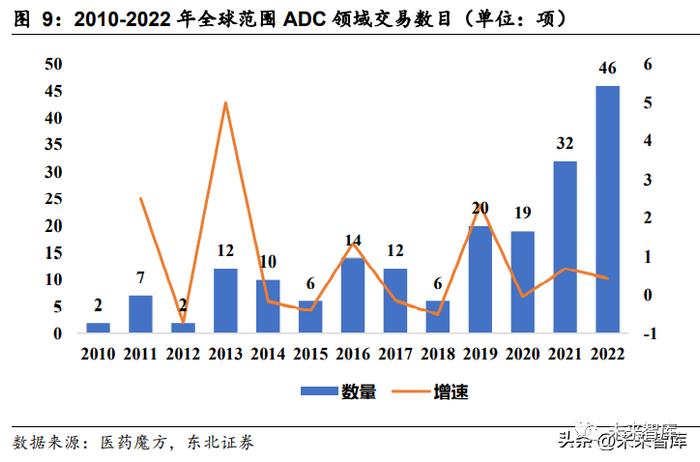
近几年来全球范围 ADC 交易频次不断攀升,2022 年完成了接近 50 次合作,总金 额超过 250 亿美元,充分证明 ADC 药物作为一种“精准投放”抗癌药物的临床价值 被广泛认可,对应临床研发即将进入高速发展时期。反观国内 ADC 管线,2022 年交易频发,验证国产创新药研发实力。2022 年 12 月, 科伦药业发布公告称与默沙东签署了合作协议,科伦博泰将其管线中七种不同在研 临床前 ADC 候选药物项目以一次性合计 1.75 亿美元不可退还的首付款,预计程碑 付款合计不超过 93 亿美元总价高额售出。此次 ADC 管线合作授权再次刷新跨国药 企交易总金额,成为目前为止总交易额最高的合作协议之一。此次合作给中国新药 出海注入了强大信心,显示了国际领域对中国药企 ADC 平台和研发能力的重要认 可。
荣昌生物为国内最早实现自主研发 ADC 产品出海企业,2021 年 8 月荣昌生物发布 公告与 Seagen 就维迪西妥单抗(RC48)的开发及商业化达成独家全球许可协议, 交易总金额达 26 亿美元的商业化合作曾一度成为 ADC 交易金额榜首。目前国内仅有少部分 ADC 企业具有授权海外 ADC 产品经验,在 19 项总交易金额 超过 10 亿美元交易中,中国药企参与仅占 7 项,自主研发产品出海 5 次,我们认 为,license out 模式一方面可以在公司发展早期的全球化开发节约资金,借助国际 药企的销售网络快速实现商业化收益。另一方面可以为企业未来产品的全面国际化, 成为国际 Big pharma 提供管理经验。在新药研发竞争日趋激烈的环境下,国内 ADC 药企需要一方面立足自主研发,另一方面积极拓展多种类型的对外合作,整合优势 资源,拓展自身平台价值。
ADC 药物 BD 交易频发体现该领域高热度,预计 BD 交易热度会继续维持。尽管目 前 ADC 产品交易仍然是 ADC 相关交易的主流,合作研发、权益转让等产品交易也 是 ADC 交易的重要组成部分。前者通过授权产品或者合作研发产品以获得共赢, 后者则多为生物技术公司授权给药企 ADC 相关技术以协助其开发药物。ADC 药物 由于其特有的模块化特点,技术交易成为了其独特的交易类型,目前许多生物技术 公司将自研的部分 ADC 技术授权给药物公司使用,进而获得首付款和销售分成, 以“技术入股”的形式探究更多临床可能性。例如荷兰的 Synaffix 公司,其拥有自研 的定点偶联技术和连接子技术,通过技术授权已经完成了共 37 亿美元的交易。随 着 CDMO 企业逐步入局 ADC 领域,通过部分自研配合技术交易实现微创新或将成 为未来 ADC 新入局玩家的方法之一。
1.4.ADC市场,大有可为
根据沙利文预测,ADC 的全球市场规模自 2017 年的 16 亿美元快速增长至 2021 年的 55 亿美元,复合年增长率为 35.9%,并预计于 2021 年至 2030 年仍将以 31.2% 的复合年增长率持续快速增长,预期于 2030 年达到 638 亿美元。从中国目前布局 管线来看,乳腺癌、非小细胞肺癌以及胃癌分别有三款产品已经进入 III 期临床关键 阶段,有望在近几年实现上市放量,看好长期市场。
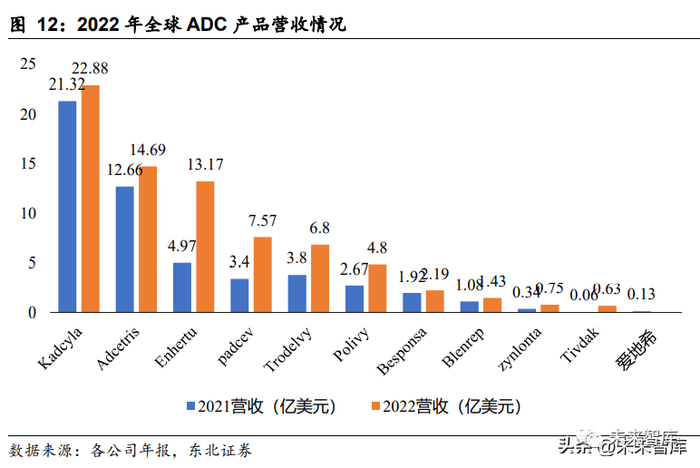
2022 年全球 ADC 市场腰部产品销售额增速较快,市场规模逐步扩充,竞争格局稳 定。2022 年 ADC 市场增长率高达 43%,Enhertu 甚至达到了 165%,一跃成为头 部产品。尽管部分产品增长迅速,但总体竞争未发生较大变化。其中,刚刚国内获 批上市的 Enhertu 得益于疗效以及适应症的不断获批,仅用两年时间成为 10 亿美 元重磅炸弹,未来 1-2 年突破 20 亿美元可期。另外,Kadcyla 增速在个位数,或是 因为上市较早,受到生物类似药的冲击以及其他 ADC 品种陆续获批。随着重磅产 品适应症以及新产品的获批,市场有望进一步扩容。国内 ADC 竞争也会日趋激烈, 随着众多企业进入 ADC 领域,如何做到差异化或是未来面临的主要问题。
从全球范围来看,ADC 处于市场快速扩张期,经过十余年的发展,ADC 产品逐渐 进入快速上市期,加上企业与医院的推广,越来越多的患者开始使用 ADC 药物, ADC 药物填补了无法耐受普通化疗药物毒性的癌症患者部分市场空缺,加之 ADC 与其他药物联用的临床试验捷报频出,ADC 药物取代化疗药物与免疫治疗联用的概 念也让其潜力进一步扩大。从区域来看,美国仍然是 ADC 药物的主要市场;由于 ADC 药物治疗费用较高的缺点,中国 ADC 市场的起步较晚,随着 ADC 药物进入 中国医保以及国产 ADC 药物入场带来的价格下降,未来中国的市场前景可观。
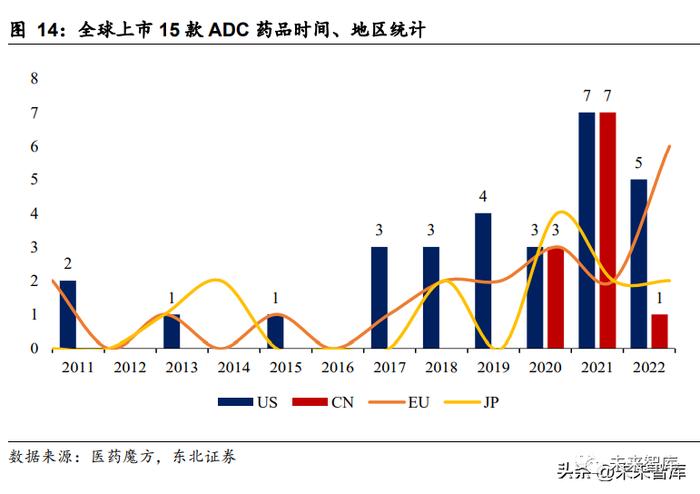
目前全球共有 15 款 ADC 药物获批上市,国内获批 7 款。截至目前,全球已有 15 款 ADC 药物获批上市:6 款用于血液肿瘤,9 款用于治疗实体瘤,靶点涉及 CD33、 CD30、CD22、CD79b、HER2、Nectin-4、Trop-2、BCMA、EGFR、CD19 和 TF。其中,5 款 ADC 药物在中国上市。Adcetris 和 Kadcyla 于 2020 年获 NMPA 批准在 中国上市,Besponsa 于 2021 年 12 月在中国获批上市。越来越多的 ADC 药物获 批激发了药企对于 ADC 的研发热情,随着临床进展的推进,未来将有更多 ADC 药 物及适应症推进到临床后期进而获批上市。
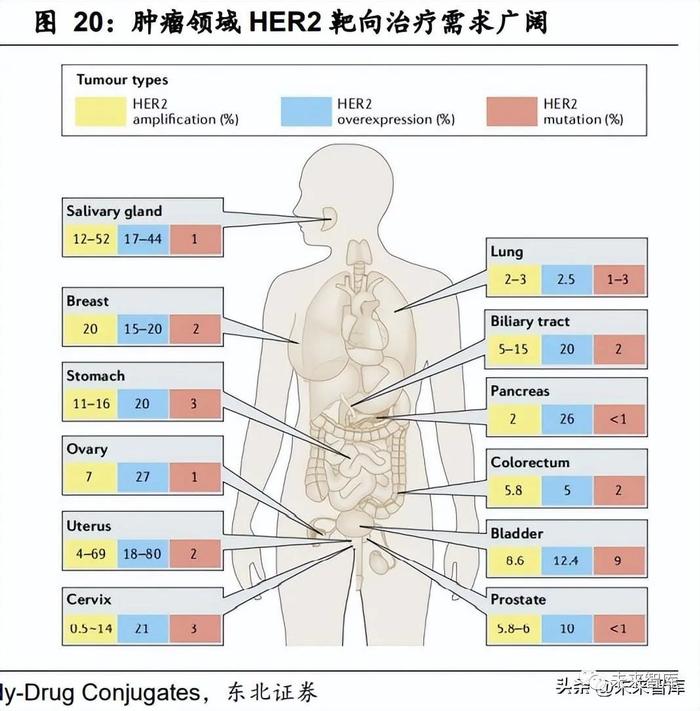
ADC 药物广泛布局肿瘤领域,国内临床需求广阔。据统计,目前全球 ADC 在研管 线重点布局在非小细胞肺癌、胃癌、卵巢癌、结直肠癌以及乳腺癌五大主要病种, 中国在研管线主要分布在非小细胞肺癌、胃癌、胃食管交界处癌、乳腺癌以及尿路 上皮癌五大瘤种。根据中国国家癌症中心发布的最新癌症报告显示,2016 年中国新增癌症病例约 406.4 万例,新增癌症死亡 241.35 万例。我国平均每天有超过 1.11 万人被诊断为新发癌症,有将近 6600 人因癌症死亡。ADC 在研管线集中布局较高 患病率领域,基于中国人口众多,有望补充现有疗法满足更大临床需求。
在目前发展的 ADC 药品在研管线中,HER2 靶点最为集中。人表皮生长因子受体 2(HER2)在正常成年人机体组织中通常低表达或不表达。众多研究表明 HER2 的 表达与多种肿瘤的发生发展密切相关。重视 HER2 检测,发展推进 HER2 靶向药 物,让患者接受更有效的“精准治疗”,有助于延长患者生存时间,ADC 药物正在向 解决临床根本需求方向快速迈进。
总体来看,靶点方面 HER2 由于其适用癌种范围广,单抗技术成熟等原因,在靶点 方面占有绝对主导,不管是临床阶段产品还是上市产品 HER2 靶点药物均超过了 25% 占比;剩余的靶点中,EGFR、Trop2、CLDN18.2 热度最高。适应症方面,目前 ADC 药物的适应症还是癌症为主,剩余的适应症集中在自身免疫病方面;癌症中,实体 瘤与血液瘤产品数量几乎相同;非癌症领域则数量极少,且大多处于临床前期,近 几年内 ADC 领域中适应症仍然会以癌症为主。
1.5.三次技术迭代造就今日ADC,治疗窗口扩充明显
ADC 药物自开发至今已有接近 100 多年历史;其首次真正尝试源于 1958 年,Mathe 将抗鼠白细胞免疫球蛋白与甲氨蝶呤偶联用于白血病的治疗,在这次尝试以失败告 终后,直到 2000 年第一款 ADC 药物 Mylotarg 才正式上市;2011 年第二款 ADC 药物维布妥昔单抗上市,自此之后的 11 年接连上市了 12 款药物。总体来说,ADC 药物从 2011 年开始才真正意义上进入了发展的快车道,开始连续且大批量的上市 药物。
三代ADC的主要区别在于抗体、连接子、毒素、偶联技术等四大基本要素。第一 代ADC 采用人源程度低的抗体分子;连接子采用不稳定的连接子;毒素采用低毒 性的药物;偶联技术使用随机偶联方式。这些基本技术要素导致第一代ADC药物 的DAR值不稳定,且毒素连接位置不固定(异质性高)、连接子断裂几率高、毒性 强,从而让能产生药效而不出现不可接受毒性的血药浓度范围(治疗窗口)很低, 需要严格控制给药剂量;又由于其采用了人源程度低的抗体,因此在血液中被免疫 系统清除的速度高,半衰期非常低,给药间隔需要很短。
第二代 ADC 采用人源化抗体;连接子采用不可裂解连接子或者可裂解稳定连接子;毒素采用澳瑞他汀类毒素或美登素类毒素;偶联方式仍然采用随机偶联技术。相较 第一代 ADC 药物,第二代 ADC 药物由于对抗体修饰程度更高,其与靶点结合能力 强,又由于其采用的连接子技术不易在血浆中断裂,因此其毒性相比一代 ADC 较 低,治疗窗口相较一代 ADC 较高;由于其采用了人源化抗体,因此其免疫原性低、 血浆半衰期高。第三代 ADC 采用完全人源化抗体或者新型抗体片段;连接子方面一般采用稳定的 可裂解连接子;毒素采用高毒性、机制创新的毒素;偶联技术一般采用定点偶联技 术。由于其采用了完全人源化抗体和血浆中稳定的连接子,因此其血浆半衰期长、 治疗窗口相较二代 ADC 更高;又由于其毒素使用种类多样,因此可以通过使用不 同机制的毒素避免耐药性发生。
截止 2023 年 3 月,共有 15 款 ADC 药物在全球上市,按照性能可以将它们分为三 代:第一代 ADC 药物是以吉妥珠单抗(Mylotarg)为代表的血液瘤 ADC;第二代 ADC 药物是以恩美曲妥珠单抗(Kadcyla)为代表的 ADC;第三代 ADC 药物是以 Enhertu、戈沙妥组单抗(Trodelvy)为代表的 ADC。
总的来说,三代 ADC 总体的差别在于其四大技术要素和众多性能指标的不同,ADC 药物演化的总体思路可以总结为:(1) 抗体方面,从鼠源抗体、低修饰程度的抗体演化到全人源抗体、修饰程度 高的抗体;(2) 连接子方面,从可裂解低稳定性连接子演化到可裂解高稳定性连接子;(3) 毒素方面,逐渐从低毒性毒素演化到高毒性毒素,并且更多的创新机制毒 素不断出现;(4) 偶联技术方面,从第三代 ADC 开始定点偶联技术逐渐成熟,越来越多新 型 ADC 药物开始使用定点偶联技术。
治疗窗口目前是评价 ADC 综合性能的最好的标准。ADC 药物的四大基本要素:抗 体(及其靶向受体)、毒素、连接子以及连接毒素的偶联技术共同决定了 ADC 药物 的八个性能指标:抗体亲和力、毒素毒性、毒素疏水性、毒素抗耐药性、连接子稳 定性、旁观者杀伤效应、DAR 值、治疗窗口等,这些指标共同决定了一款 ADC 药 物的性能以及治疗效果。其中,ADC 药物的开发具有较高的技术壁垒,理论上较高 的 DAR 值对应更强的药效,然而随着 DAR 值增加,ADC 的疏水性以及抗体分子 天然结构受到的影响也会增加,最终导致药物分子的清除率增高,体内半衰期降低。
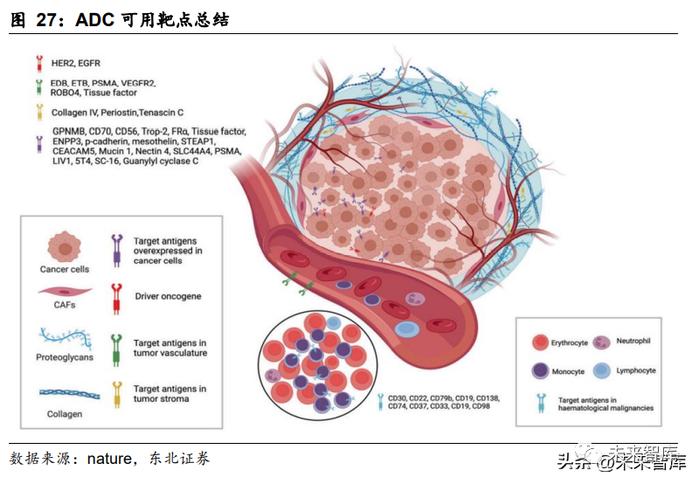
不同偶联技术决定药物-抗体比(DAR 值),治疗窗口为评价 ADC 综合性能的重要 标准。药物-抗体比(DAR 值)是指抗体所连接药物数量的平均值,它是能够表征 ADC 药物高效低毒性,即治疗窗口的重要属性。ADC 药物作为一种基于化疗药物连接抗 体,通过抗体靶向性抵消化疗药物对普通细胞的毒副作用,同时解决抗体药物耐受 剂量高但治疗作用较差缺点的新型药物,量化指标治疗窗口是目前评判 ADC 药物 能否实现高效靶向杀伤的重要标准。治疗窗口越宽泛,ADC 药物的药效以及安全性 越好,即达到 ADC 通过结合高效细胞毒性药物与靶标特异性抗体将细胞毒性药物 直接送达病变组织,同时限制药物在非目标组织中毒性的效果。
2.ADC药物协同共赢的技术核心—抗体、连接子、毒素、偶联技术
具体来说,ADC 药物治疗肿瘤类疾病主要通过抗体带来的细胞毒作用、受体干扰作 用,以及效应分子的细胞毒性两方面实现。其中,抗体的细胞毒作用又分为抗体依 赖的细胞毒性作用(ADCC)、补体依赖性细胞毒性作用(CDC)、抗体介导的胞吞作用 (ADCP)三种;效应分子的杀伤效应可以分为直接杀伤和旁观者杀伤效应(Bystander killing effect)两种途径。
在这些机制中,最主要的杀伤途径还是来自于毒素的直接杀伤以及旁观者杀伤效应。典型的 ADC 药物由于大多采用内化后释放毒素的方式,为了促进其内化,会刻意 的修饰抗体的 Fc 段以适当削弱其免疫作用,但是也有新型的 ADC 药物将抗体的免 疫作用提高,配合胞外释放毒素实现免疫杀伤、毒素杀伤结合的设计。目前的 ADC 创新药物设计均在尽可能的增加其旁观者杀伤效应,实现治疗的高效性。
2.1.抗体与靶抗原—ADC的制导系统
2.1.1.ADC靶点的选择
ADC 的靶点直接决定了 ADC 药物分子的作用机制与适应症,但同时可能带来相对 应的靶点毒性。解决靶点毒性,除了选择低毒靶点以外,还可以针对抗体进行筛选 改造,制造出精确靶向肿瘤细胞靶点的抗体,因此靶点毒性与靶点选择、抗体筛选 密切相关。
一般来说,ADC 药物靶向抗原的挑选有以下原则:1、肿瘤组织中高度表达,正常组织少量表达或不表达:直接影响 ADC 靶点毒性的 强弱,若 ADC 分子结合到了正常组织中的靶点,会导致正常组织的严重损伤,例如 Trop-2 靶点会在上皮细胞中高度表达,未选择合适的抗体可能会导致皮疹等严重皮 肤副作用。2、抗原不会从肿瘤细胞脱落进入血浆;保证 ADC 小分子高效靶向性、避免毒性。3、抗原可以介导 ADC 分子内化:ADC 内化效率直接决定了 ADC 的杀伤效率。由 于目前 ADC 基本采用内化后脱落毒素的机制,因此需要选择内化效率高的靶点。如果靶点的内化效率低下,可能会导致药物在血浆中被代谢后仍然没有足量药物进入并杀伤靶细胞;但靶点的内化效率低也可以通过抗体弥补,如果筛选出高内化速 度的抗体,可以弥补一部分靶点的低内吞效率。
2.1.2.ADC抗体的选择
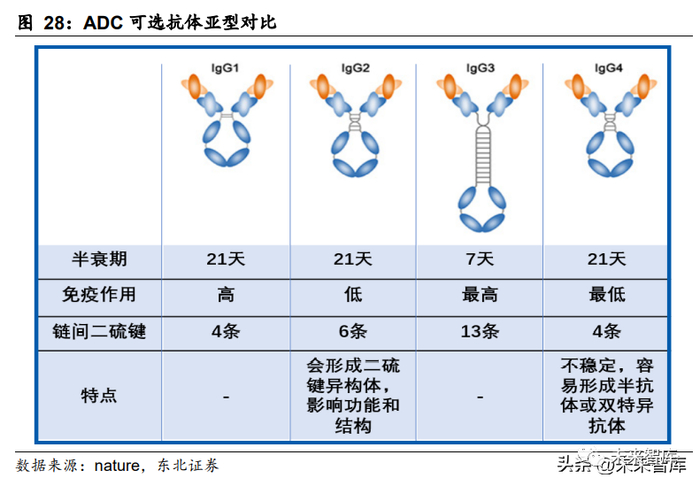
ADC 抗体决定了 ADC 的靶向能力强弱,抗体的挑选原则主要有以下几点:1.与靶 点结合能力高;2.能够快速内化;3.低免疫原性;4.血浆半衰期长。免疫原性主要与 抗体人源化程度有关,如果选择人源化程度低的抗体可能会导致人体自身免疫系统 的免疫反应从而带来副作用且降低半衰期。半衰期则主要影响 ADC 的给药频率和 药效,由于 ADC 药物进入身体后绝大多数停留在血浆中,只有约 1%的分子会进入 肿瘤组织,因此半衰期长的 ADC 能够在血浆中停留更长的时间,从而有更多的机 会进入肿瘤组织并杀死肿瘤细胞,因此半衰期长的 ADC 能有更好的疗效以及更长 的给药频率。IgG 有 4 种亚型,其中,IgG1 是 ADC 应用最多的抗体亚型,由于其半衰期长、渗 透性较好、免疫作用强,因此基本所有 ADC 药物均选择 IgG1 抗体。
抗体按照人源化程度可以将抗体分为鼠抗体、嵌合抗体、人源化抗体,随着人源化 程度加强,抗体免疫原性降低、半衰期变长,但是亲和力会变差。目前 ADC 药物除 了少数(Adcetris、Lumoxiti、Akalux、Zynlonta)治疗血液瘤的药物选用鼠抗体或 嵌合抗体外,其他均选用人源化的抗体。由于血液瘤病灶即在血液中,因此选用亲和力强但是半衰期短的非人源抗体效果并不差,但是实体瘤中由于抗体难以渗透到 肿瘤组织,一般选用高度人源化抗体以尽量提高渗透性。
3.前沿技术的选择:抗体的前沿技术主要有以下几点:糖基化修饰、抗体片段、前 抗体、双特异性抗体。从目前的研究状况来看,糖基化修饰目前主要应用于单抗产 品上,ADC 药物并没有使用该技术的产品;抗体片段已经有鲁莫西替等产品使用, 且技术较为成熟。前抗体、双特异性抗体目前处于临床探索阶段,如 ZW49、CX2029 等临床阶段的产品采用了这些技术。
2.2.毒素—ADC的杀伤系
2.2.1.ADC毒素的挑选原则
ADC 的弹头(毒素)直接决定了 ADC 药物杀伤肿瘤细胞的机制、能力等关键因素, 是 ADC 药物最核心的因素。理想的 ADC 毒素需要同时具备对肿瘤细胞的高效杀伤 性以及在正常组织中的安全性。ADC 的毒素有以下几个挑选原则:1.药理机制明确;2.对肿瘤细胞毒性极高;3.能 够被化学修饰以调整其性能;4.正常组织中毒副作用低。
2.2.2.ADC常用毒素介绍
目前 ADC 常用的毒素主要有两大类:微管抑制剂类、DNA 损伤剂类,除此之外还 有一些创新性机制的新型毒素。1、 微管抑制剂类:所有微管抑制剂的作用机制都很相似,通过阻断微管蛋白组装 从而让细胞分裂停滞在 G2/M 期从而诱导细胞凋亡。正式由于其机制使其只能 作用于分裂期的细胞,无法有效杀伤静止期癌细胞。目前微管抑制剂主要有 3 小类:澳瑞他汀类、美登素类、Tubulysin 类。
2、 DNA 损伤剂类:DNA 损伤剂的机制有两种:第一种是靶向 DNA 的小沟,分别 通过断裂单烷基腺嘌呤碱基或交联鸟嘌呤碱基来让 DNA 损伤,从而杀死靶细 胞;第二种是作用于 DNA 拓扑异构酶 I 上从而导致细胞死亡。目前 DNA 损伤 剂大类中主要有 3 小类药物:卡奇霉素类(Calicheamicin)、安曲霉素类(PBD)、 喜树碱类,前两种均是靶向 DNA 小沟的损伤剂,喜树碱类是 DNA 拓扑异构酶 I 抑制剂。
3、 创新机制毒素:创新类毒素分为物理毒素和新型化学毒素,其中物理毒素有核 素、光敏性毒素等;新型化学毒素有蛋白质合成抑制剂等毒素。目前通用的毒素中,PBD 毒性最高,IC50(某种药物诱导肿瘤细胞凋亡 50%的浓 度)可以达到 10-11 以下,其次是美登素类、澳瑞他汀类、喜树碱类。其中,喜树碱 类毒性偏低,某些ADC 如Trodelvy使用的SN38 其实是伊利替康的活性代谢产物, 毒性与一般化疗药物无异。
影响毒素能否发挥旁观者杀伤效应的因素主要有两点:连接子能否裂解、毒素能否 穿膜。其中毒素能否穿膜是决定性因素,就算使用可提前裂解的连接子让毒素在肿 瘤微环境中提前释放,如果毒素无法透过细胞膜达到其发挥作用的细胞器,药物仍 然无法实现范围杀伤。而毒素能否穿膜的决定性因素就是毒素疏水性的强弱,一般 而言疏水性强的毒素跨膜能力强,反之亲水性越强跨膜能力越弱。疏水性强的毒素 如 MMAE、DM4、Tubulysin、PBD 类、喜树碱类、卡奇霉素类等毒素一般搭配可 裂解连接子充分释放其旁观者杀伤效应的潜力;而亲水性强的毒素如 MMAF、DM1、 α-鹅膏蕈碱等一般搭配不可裂解连接子增强其稳定性。
一般而言肿瘤细胞的耐药性的产生是由于一种跨膜转运蛋白多药耐药蛋白 1 (MDR1)的表达,其具有转运疏水化合物的特性。因此,疏水性过高的药物在治 疗进行一段时间后可能会出现耐药性,而亲水性强的药物基本不会有耐药性。
2.3.连接子与偶联技术—ADC稳定性的关键因素
2.3.1.连接子的挑选原则和类型
连接子由三部分组成:隔离棒、裂解区、释放区。其中,裂解区是连接子的核心, 连接子的断裂部位发生在裂解区;隔离棒和释放区的作用都是修饰亲水/疏水性,一 般会采用 MC(马来酰亚胺己酰基)、PEG(聚乙二醇)、PABC(对氨基苯甲醇)。其中释放区会在连接子断裂后与毒素一起释放,因此释放区还可以修饰连接子断裂 后毒素的亲水/疏水性。连接子的挑选原则主要有以下几点:1.血液中足够稳定;2.ADC 被内吞或达到肿瘤 组织后能有效断裂;3.能够给 ADC 整体带来亲水/疏水性修饰。其中第三点尤为重 要,因为如果 ADC 毒素端的亲水性过强,再血液中会相互聚合成团从而无法发挥 作用,因此修饰亲水/疏水性是连接子的重大作用之一。
2.3.2.ADC偶联技术的介绍以及DAR值
偶联技术是影响 ADC 药物 DAR 值的决定性因素,也是 ADC 药物技术开发最为困 难的壁垒。目前偶联技术可以分为非定点偶联技术、定点偶联技术两大类。其中非 定点偶联技术可以分为基于赖氨酸的偶联技术和基于半胱氨酸的偶联技术;定点偶 联技术目前主流的有链间半胱氨酸定点偶联技术、工程化突变半胱氨酸偶联(Thio-mab)技术、非天然氨基酸偶联技术、酶促偶联技术、糖基偶联技术、临近诱导抗 体偶联(pClick)技术几种。偶联技术选择的标准有工艺简洁性、方法通用性两点。如果一种偶联技术的工艺成本足够低,适配的连接子、毒素类型足够普遍,就能够 被应用于大批量生产。目前随着第三代 ADC 时代的到来,定点偶联技术已经成为 ADC 技术发展的趋势,越来越多的企业开始自研或引入偶联技术以提高 ADC 的性 能。
1.基于赖氨酸的偶联技术:抗体表面赖氨酸能和连接子上的 MC 反应可以构建 ADC。但是抗体中可以连接的位点超过 20 个,所以这些位点的偶联导致异质混合物的产 生,因此采用赖氨酸偶联得到的 ADC 异质性较强。目前赖氨酸偶联技术能生成 DAR=0-8 的 ADC 药物,采用赖氨酸偶联的药物有 Mylotarg、Kadcyla、Besponsa、 Akalux 四种。2.基于半胱氨酸的偶联技术:抗体上的半胱氨酸还原后的二硫键和连接子上的 MC 发生反应可以构建 ADC。一个抗体中有 16 对二硫键,其中 12 对为链内,4 对为链 间,其中链间二硫键是应用最多的位点。半胱氨酸偶联可以显着降低 ADC 的异质 性,以及获得比基于赖氨酸偶联的 ADC 更高的均一性。目前半胱氨酸偶联技术能 生成 DAR=0-8 的药物,采用半胱氨酸偶联技术的 ADC 有 Adcetris、Polivy、Padcev、 Blenrep、Zynlonta、RC48、Tivdak 等药物。
3.链间半胱氨酸定点偶联技术:链间半胱氨酸定点偶联技术通过将抗体链间的 4 对 二硫键全部还原后连接毒素,可以得到 DAR=8 且位点相同的 ADC。虽然实现了定 点偶联的效果,但其实链间半胱氨酸全还原仍然使用了非定点欧联的技术手段,并 且只能产生 DAR=8 的产物。目前使用该技术的药物有 Enhertu、Trodelvy。4.工程化突变半胱氨酸偶联(Thio-mab)技术:工程化突变半胱氨酸偶联技术通过 将抗体一些指定位点的氨基酸突变为半胱氨酸后将半胱氨酸还原出二硫键然后连 接毒素。一般来说该偶联方式生产的药物 DAR=2,但也可以通过突变不同位点改变 DAR 值。
5.非天然氨基酸偶联技术:该技术通过在抗体的原始序列中人为加入非天然氨基酸, 使其在抗体表面呈现可方便偶联的特异性位点,进而获得位点确定,DAR 值均一的ADC。非天然氨基酸偶联可以随意突变非天然氨基酸,并且得到 DAR 值任意的 ADC。6.酶促偶联技术:酶促偶联技术需要构造特定的工程性酶,同时要在抗体上引入特 定位点,通过工程性酶催化抗体与连接子连接生成 ADC。该技术同样可以选择位点, 得到任意 DAR 值的 ADC。
7.糖基偶联技术:通过用糖苷内切酶修饰天然蛋白质中不同的糖基而曝露出 N-乙酰 氨基葡萄糖,然后经叠氮修饰后的 N-乙酰半乳糖胺利用糖基转移酶连接到抗体的 N-乙酰氨基葡萄糖上,最后发生点击化学反应可以得到定点偶连的 ADC。这种方 法同样可以获得任何 DAR 值的 ADC。8.临近诱导抗体偶联(pClick)技术:临近诱导技术的特点是无需对抗体进行任何 改造,而是将毒素-连接子与抗体亲和蛋白相连,然后让抗体亲和蛋白再与抗体进行 临近诱导反应,从而获得任意 DAR 值的 ADC 分子。
2.3.3.ADC药物DAR值的选择
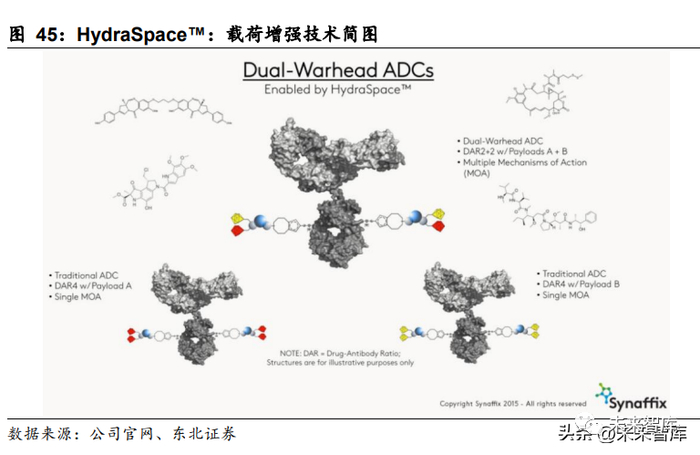
药抗比(DAR)以及其分布范围,以及每个药物的偶联位置对 ADC 分子的稳定性、 治疗窗都有重要影响。理论上较高的 DAR 值对应更强的药效,然而随着 DAR 值增 加,ADC 的疏水性以及抗体分子天然结构受到的影响也会增加,最终导致药物分子 的清除率增高,体内半衰期降低,以及药物毒性提高。目前获得 DAR 值均一的 ADC 有两种途径:采用非定点偶联技术然后进行层析分离纯化获得、采用定点偶联技术 直接获得。
2.4.海外核心ADC药物平台—Seagen
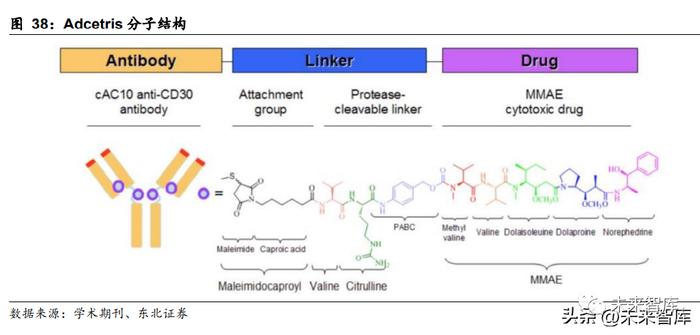
Seagen 的药物平台有两个核心化合物:Vedotin、Mafodotin。其中,Vedotin 分子 采用 MMAE 毒素;Mafodotin 分子采用 MMAF 毒素,两个平台的区别在于稳定性 高低与旁观者效应的有无。Vedotin 平台最早来源于 Seagen 前身 Seattle Genetics 与 BMS 合作研发出的 MMAE 毒素,随后公司研发出了 MC-VC-PABC 的蛋白酶可裂解连接子,从而构成 了 Vedotin 平台,分子式为 MC-VC-PABC-MMAE。同时,该平台采用半胱氨酸随 机偶联技术,配合分离纯化可以生产 DAR=0-8 的均一 DAR 值随机位点的 ADC 分 子。该平台药物的性能特点是:1.毒素杀伤性适中,一般采取 DAR=4;2.药物拥有 优秀的旁观者杀伤效应;3.药物适应症既可以为实体瘤也可以为血液瘤,抗体也可 以任意选择。
该平台一共拥有 Adcetris、Polivy、Padcev、RC48、Tivdak 五款上市药物。其中 Adcetris、Padcev、Tivdak 目前为 Seagen 持有权益,Polivy 是 Seagen 与罗氏合 作开发的药物,RC48 是荣昌生物绕过专利保护后研发随后被 Seagen 买入海外权 益的药物。
Mafodotin 药物平台由不可裂解连接子 MC 与 MMAF 毒素组成。由于 MMAF 在细 胞内会被自然的处理为离子形式,再加上 MC 的稳定性,Mafodotin 平台的药物基 本没有任何旁观者杀伤效应,但与此同时其稳定性也非常高。由于 MC 在偶联反应 中的泛用性,Mafodotin 平台也可以通过半胱氨酸随机偶联技术产生 DAR=0-8 任意数值的 DAR 值均一、偶联位点不均一的 ADC。同时,其也可以选择任意类型的抗 体,靶向任意肿瘤适应症。该平台目前只有 Blenrep 一款药物,该药物为 Seagen 与 GSK 合作开发。
数值的 DAR 值均一、偶联位点不均一的 ADC。同时,其也可以选择任意类型的抗 体,靶向任意肿瘤适应症。该平台目前只有 Blenrep 一款药物,该药物为 Seagen 与 GSK 合作开发。已有多个核心临床试验证明 Adcetris 治疗淋巴瘤的高效。Adcetris 不仅获得 FDA 突 破性疗法认证,引入国内后也被选入如“抗体药物偶联物治疗恶性肿瘤临床应用专家 共识(2020 版)”等多个专家共识推荐中。
2.5.海外核心ADC药物平台—第一三共
第一三共目前拥有一个 ADC 药物平台,核心分子是其独创的依喜替康类似物 Dxd 毒素,辅以其自研的 GGFG 蛋白酶可裂解四肽连接子,共同组成 Deruxtecan 化合 物。同时,其偶联方式一般选用链间半胱氨酸定点偶联技术,通过将链间的半胱氨 酸全部还原露出 8 个二硫键然后连接 8 个毒素分子,形成 DAR=8 的均一 DAR 值 均一位点 ADC。目前第一三共只有一款 ADC 上市,即 Enhertu(德喜曲妥珠单抗)。其于 2019 年 上市,但 2021 年销售额已经达到 5.43 亿美元,位居 ADC 药物中销售额第 3,实 体瘤 ADC 销售额第二。多家分析机构预计其于 2025 年之前销售额将会超过目前 ADC 销售额第一的恩美曲妥珠单抗。
德喜曲妥珠单抗由人源化 HER2 抗体曲妥珠单抗通过蛋白酶可裂解连接子 GGPG 与喜树碱类似物 Dxd 连接而成,同时其采用链间半胱氨酸全还原偶联方式,DAR 值 为稳定的 8。
Enhertu 的亮眼之处主要有以下两点:1.适应症广泛,基本涵盖了所有主流实体瘤。2.效能高,对多个适应症的疗效均高于目前最有效的恩美曲妥珠。首先是乳腺癌适 应症,第一三共以 DESTINY-Breast 系列为名进行了 8 个关键临床试验。在这 8 个 临床实验中最重要的有三个:首先是 DESTINY-Breast01,Enhertu 依靠此临床实 验结果通过了 FDA 的 NDA 申报。其次是 DESTINY-Breast03,Enhertu 依靠此头 对头实验证明了其有效性优于当前主流的 HER2 ADC 恩美曲妥珠。最后是 DESTINY-Breast04,在该临床试验中 Enhertu 首次被应用于 HER2 低表达乳腺癌, 证明了其对乳腺癌治疗的广泛性。
同时,Enhertu 还在胃癌、非小细胞肺癌领域有优秀效果,第一三共分别在 2021 年 和 2022 年公布了 Enhertu 在非小细胞肺癌、胃癌领域的临床结果。在非小细胞肺 癌领域 Enhertu 还获得了 FDA 的突破性疗法认定。总的来看,Enhertu 是一款潜力 极大的实体瘤 ADC 产品,由于其出色的疗效和广泛的适应症,其在实体瘤领域的 竞争力已经超过目前唯一的对手恩美曲妥珠。未来,实体瘤领域 ADC 新产品必定 无法逃脱与 Enhertu 头对头的比较,实体瘤领域 ADC 的竞争已然来到“一超多强”的新格局。
2.6.ADC技术平台介绍—Synaffix技术
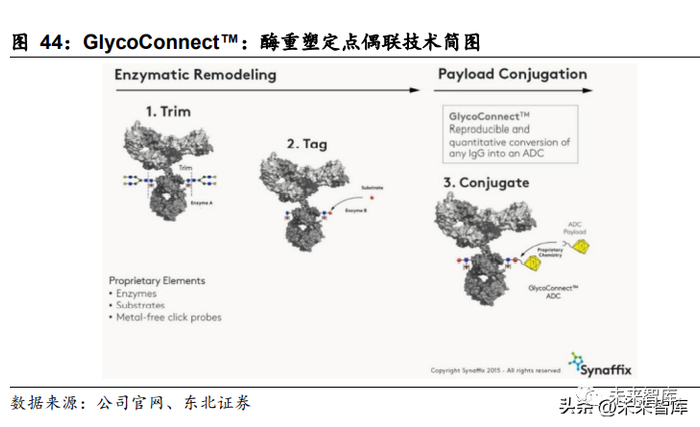
ADC 药物由于模块化强,因此研发、生产外包率很高。因此,部分拥有 ADC 研发 或生产技术的企业选择作为 CMO/CRO/CDMO 方为药企提供服务。目前主要有两 种技术合作方式:纯技术平台(CRO 模式)、CDMO 模式。其中代表企业分别是 Synaffix 和药明康德。Synaffix BV 是荷兰一家生物技术公司,专注于进行 ADC 药物技术授权工作,到目 前为止,其合作伙伴包括 ADC therapeutics、Mersana therapeutics、美雅珂、 Miracogen、信达生物、普方生物等药企。其中最高合作金额已经超过 5.68 亿美元。GlycoConnect™:酶重塑定点偶联是一种定点欧联技术,应用天然糖基化位点实现 定点偶联。其专利中披露了一种利用内切糖苷酶对 N-乙酰葡糖胺的抗体聚糖进行去 糖基化,得到包含 N-乙酰葡糖胺取代基的抗体。通过 Synaffix 研发的两种工程化改 造酶,来实现定点、定 DAR 值偶联。
(本文仅供参考,不代表我们的任何投资建议。如需使用相关信息,请参阅报告原文。)

