(报告出品方/作者:中银证券,邓周宇)
1 新冠病毒变异逐渐削弱现有疫苗有效保护率
变异定义及作用原理
病毒变异指的是部分病毒的遗传信息发生了改变。病毒在感染其他细胞后,将自身的遗传信息(DNA 或 RNA)注入宿主细胞内,并开始分裂增殖。在分裂增殖的过程中,遗传信息可能会发生随机的“笔 误”,导致新的病毒携带了有所不同的遗传信息,这一过程被称为变异。由于变异是随机的,因此 有些变异可能会使病毒更易被降解、有些可能会降低传染性,有一些则相反,可能会增强病毒的毒 性、传染性。病毒复制频次越高,出现变异的次数也越高。变异次数越高,则发生加强病毒传染性、 毒性等危害的变异就有更大可能出现。因此,当病毒流行程度越来越高,出现难缠的变异株的可能 性就越大。
系列报告中上一篇介绍了人体免疫系统和疫苗工作的一般性原理。人体免疫系统可分为固有性和获 得性免疫。固有性免疫是人体天生带有的免疫系统,具有非特异性、反应快速等特点。获得性免疫 则具有特异性,在首次感染时反应较慢,待首次感染人体产生免疫记忆后,二次感染时特异免疫将 能够快速启动清除感染源,此时获得性免疫杀伤效率高于固有免疫。疫苗的作用便是激活获得性免 疫,在去除毒性的前提下使人体免疫系统能够形成特异性的免疫记忆。

根据上述介绍,疫苗激活的获得性免疫是特异性的,当病毒抗原发生变化时,人体的免疫记忆和变 异病毒的匹配度下降,可能导致免疫系统无法识别变异病毒。因此疫苗应对变异病毒的有效率便会 下降。随着病毒变异,任何疫苗种类均会出现类似的免疫逃逸情况,但不同技术路线、不同变异株 免疫逃逸的程度有所不同。
在本次新冠疫情中,第一代的原型病毒已逐渐被众多变异株所取代,这也对已上市甚至处于临床阶 段的新冠疫苗带来了不小挑战。2021 年中 CureVac 发布的临床数据显示,公司 mRNA 疫苗临床实验 中,所有感染者中只有 1%感染的是第一代原型病毒。同时公司也将临床失败的主要原因归结于变异 株的大肆流行,使得原本针对第一代病毒研制的疫苗有效率大幅下降。
根据 WHO 的信息,各主流疫苗的保护率如下:牛津/阿斯利康 AZD1222 对有症状感染保护率 63.09%;强生的 Ad26.CoV2.S 有症状感染保护率 66.9%,重症保护率为 85.4%,住院保护率为 93.1%;摩德纳 Moderna 保护率为 94.1%;BioNTech 的 BNT162b2 有症状感染保护率为 95%;科兴新冠疫苗有症状感染 保护率为 51%,重症保护率为 100%;国药新冠疫苗有症状感染保护率为 79%。
2 刺突蛋白与RBD:新冠疫苗的优秀靶点
新型冠状病毒(SARS-CoV-2)是一种正向单链的 RNA 病毒。与其他病毒相似,新冠病毒拥有蛋白外 壳和被包裹于中央的遗传物质内核。新闻中,我们常常听到某重组蛋白疫苗或核酸疫苗采用了全长 S 蛋白或 RBD 作为疫苗表达的目标,在此部分,我们简单介绍了 S 蛋白与 RBD 的特征以及作用,同 时尝试分析不同的选择可能对疫苗产生的影响。
S 蛋白:新冠病毒入侵武器,大范围搜寻半径及灵活性给予强传染性
新冠病毒的感染路径依赖于刺突蛋白(S 蛋白)。病毒进入人体后,S 蛋白搜寻人体细胞表面的 ACE2 受体,并与其结合,使病毒的遗传物质得以进入人体细胞,并破坏人体细胞本身的遗传复制,转而 大量复制并生产病毒。S 蛋白分为两个亚单位部分:S1 和 S2。S1 包括了受体结合域(Receptor binding domain,RBD)。RBD 位于 S 蛋白头部,负责识别人体细胞上的 ACE2 受体。RBD 同时也是中和抗体的一个重要靶点,中和 抗体通过与 RBD 结合,使其丧失与 ACE2 受体的结合能力。因此,S1 亚单位和 RBD 是疫苗开发的重 中之重。
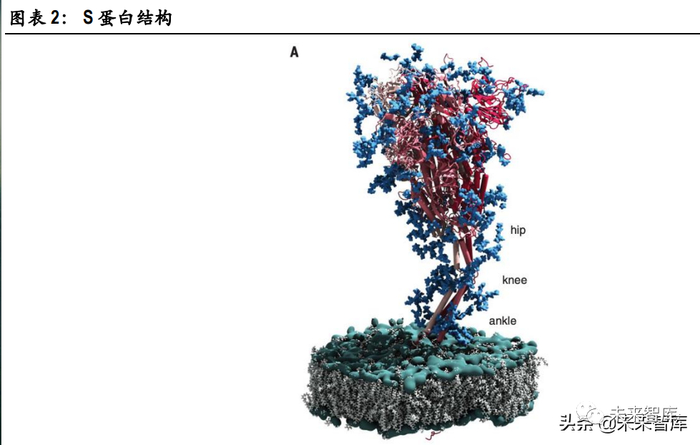
当 S 蛋白的 RBD 与人体细胞受体配对后,病毒壳膜与人体细胞膜逐渐融合,使病毒的遗传物质能够 自由进入人体细胞,并开始复制繁殖。这一过程就是我们常说的病毒感染。
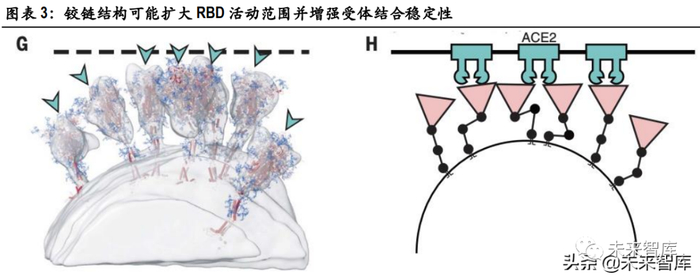
S 蛋白具有铰链结构,因此非常灵活。S 蛋白可分为 4 个部分,3 个连接关节:臀部(hip)、膝部(knee)、 ankle(踝部)。连接关节可大角度扭动,使 S 蛋白头部具有很大的活动空间和方向自由,因此,S 蛋白可能拥有更大的搜寻面积。同时,由于 S 蛋白可以通过铰链调整 RBD 与受体的连接姿态,因此, 病毒蛋白与人体细胞受体连接更为稳固,使病毒能够从容不迫地开始感染过程。粉色三角结构为 S 蛋白与人体细胞结合区域,黑点为三个可灵活扭动的连接关节,S 蛋白可通过连 接关节的姿态调整,保持与人体细胞 ACE2 受体稳定的连接,延长病毒壳膜与人体细胞膜的融合时间 窗口。
S 蛋白:变异特征
新冠病毒基因组稳定性较差,更容易积累变异,其变异积累速率约为每年 9.8× 10−4替代/位点。截至 2021 年 5 月初,共有约 140 万个变异序列被报告并收录至 Global Initiative on Sharing Avian Infuenza Data (GISAID),其中 3913 个被定义为具有代表性的主要变异基因组。然而,并非所有变异都会造成病毒传 染性、传染机理或其他属性的重大变化,所以并非任何变异株都会成为主流株型之一。以目前情况 来看,对疫苗或康复者血清的有效性造成重大影响的变异主要发生在刺突蛋白(S 蛋白)。由于 S 蛋白是新冠病毒传染机制的重要组成部分,因此,发生在 S 蛋白的突变更有可能造成病毒传染感染 属性的改变,更容易使病毒逃脱人体免疫的识别,无论是自然感染产生的特异免疫或是疫苗激活的 免疫。


当 S 蛋白的 RBD 与人体细胞受体配对后,病毒壳膜与人体细胞膜逐渐融合,使病毒的遗传物质能够 自由进入人体细胞,并开始复制繁殖。这一过程就是我们常说的病毒感染。
S 蛋白具有铰链结构,因此非常灵活。S 蛋白可分为 4 个部分,3 个连接关节:臀部(hip)、膝部(knee)、 ankle(踝部)。连接关节可大角度扭动,使 S 蛋白头部具有很大的活动空间和方向自由,因此,S 蛋白可能拥有更大的搜寻面积。同时,由于 S 蛋白可以通过铰链调整 RBD 与受体的连接姿态,因此, 病毒蛋白与人体细胞受体连接更为稳固,使病毒能够从容不迫地开始感染过程。粉色三角结构为 S 蛋白与人体细胞结合区域,黑点为三个可灵活扭动的连接关节,S 蛋白可通过连 接关节的姿态调整,保持与人体细胞 ACE2 受体稳定的连接,延长病毒壳膜与人体细胞膜的融合时间 窗口。

S 蛋白:变异特征
新冠病毒基因组稳定性较差,更容易积累变异,其变异积累速率约为每年 9.8× 10−4替代/位点。截至 2021 年 5 月初,共有约 140 万个变异序列被报告并收录至 Global Initiative on Sharing Avian Infuenza Data (GISAID),其中 3913 个被定义为具有代表性的主要变异基因组。然而,并非所有变异都会造成病毒传 染性、传染机理或其他属性的重大变化,所以并非任何变异株都会成为主流株型之一。以目前情况 来看,对疫苗或康复者血清的有效性造成重大影响的变异主要发生在刺突蛋白(S 蛋白)。由于 S 蛋白是新冠病毒传染机制的重要组成部分,因此,发生在 S 蛋白的突变更有可能造成病毒传染感染 属性的改变,更容易使病毒逃脱人体免疫的识别,无论是自然感染产生的特异免疫或是疫苗激活的 免疫。
S 蛋白本质是由 1273 个氨基酸组成的多肽。S1 与 S2 的边界位于第 685 个氨基酸。RBD 编码区域为第 331 至第 524 个氨基酸之间的肽链片段,占 S 蛋白总长度的 15.2%。截至 2021 年 2 月 3 日,GISAID 记 录了 5106 个不同的氨基酸替代变异,它们发生在 1267 个不同位点上。1267/1273,此数据表明几乎所 有的位点都可能会发生变异,且其中不包括插入或删减变异。5106 个替代变异中,161 个被认为会显 著影响血清中抗体对其的识别能力。
3 MRNA新冠疫苗真实世界数据解析:高保护率应证
mRNA 疫苗的临床运用开始于 2020 年新冠疫情。辉瑞/复星/BioNTech 联合研发的 BNT162b2,以及由 Moderna 研发的 mRNA-1273 是全球最早广泛使用的 mRNA 疫苗。
III 期临床数据展现优秀的有效性
2020年 11 月 18 日,辉瑞发布了 BNT162b2的 III期临床试验结果,结果显示疫苗整体保护率高达约 95%。2021 年 3 月 31 日,Moderna 发布了 mRNA-1273 的 III 期临床试验结果,结果显示疫苗整体保护率也达 到 94.1%,与 BNT162b2 的数据非常接近。同时,mRNA 疫苗在 65 岁及以上的老年群体中的保护率仍 旧接近 90%,能够高效地激发免疫反应。

辉瑞/BioNTech mRNA 疫苗(BNT162b2)有效性
临床试验数据分为两部分。第一部分,样本人群为在实验前或实验开始时均未感染新冠病毒的人群, 本样本人群共有 36523 人。在完成 2 剂接种 7 天后,疫苗有效保护率达到 95.0%。第二部分样本人群包括感染和未感染新冠病毒的人群,样本人数 40137 人。疫苗有效保护率达到 94.6%。根据年龄段划分,BNT162b2 对 16-64 岁人群的保护率为 95.1%,对 65 岁及以上的老年群体保护率则维 持在了 94.7%。数据显示了 mRNA 疫苗在人群中激活免疫系统的能力基本不受接种者年龄的影响。
Moderna mRNA 疫苗(mRNA-1273)有效性
Moderna 公司与美国国家过敏及传染疾病研究所(NIAID)研发的 mRNA-1273 也给出了相似的 III 期临床 结果。在本次针对 18 岁以上人群的临床试验中,样本人数为 28207 人。在完成第 2 剂接种 14 天后, 测得 mRNA1273 疫苗保护率约为 94.1%(95%CI:89.3%-96.8%)。在 3583 位 65 岁及以上的老年人群样本中,测得疫苗保护率为 86.4%,维持在较高水平。
Moderna 于 2021 年上半年业绩发布会上披露了 mRNA-1273 最终的 III 期临床实验结果。COVE 分析数据 显示,mRNA-1273 能够提供 93.2%的整体保护率(95%CI:91.0-94.8%);98.2%的重症保护率(95%CI:92.8%-99.6%);100%的死亡保护率。同时,mRNA-1273 展现了较为持久的保护力。接种第二针 14 天后,疫苗整体保护率为 93.1%。细分时 段:接种第二剂 14 天后,且不超过 2 个月期间,保护率为 91.8%;接种第二剂 2 个月后,且不超过 4 个月期间,保护率为 94.0%;接种第二剂 4 个月后,保护率为 92.4%。
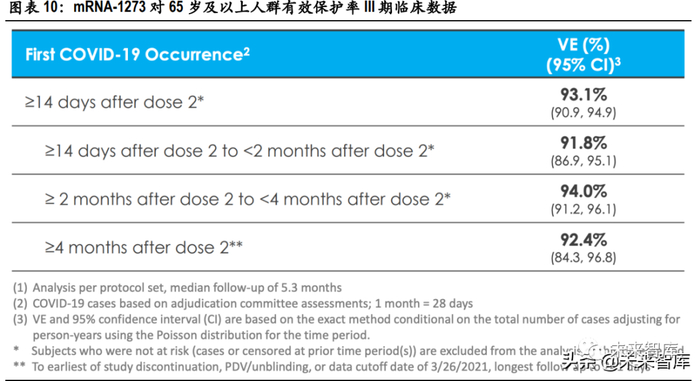
III 期临床数据显示 mRNA 疫苗对新冠病毒的保护率高达 94%以上,国药传统灭活疫苗的保护率虽 远远高于 WHO 和 FDA 建议标准的 50%,但仍与 mRNA 疫苗差距明显。同时,mRNA 疫苗对 65 岁 及以上的老年群体的保护作用也非常可观:BNT162b2 对 64 岁以上群体的保护率为 94.7%,仅比 16-64 岁群体数据低 0.4%。Moderna 的 mRNA1273 对 64 岁以上人群的保护率为 86.4%,甚至高于灭 活疫苗的整体保护率。(报告来源:未来智库)
真实世界数据应证 mRNA 疫苗高保护率,仍能有效应对变异株
随着 BNT162b2 和 mRNA1273 在全球多个国家开始接种,mRNA 疫苗真实世界保护率(Effectiveness)开 始揭开面纱。目前,BNT162b2 已在全球大范围接种。近期,不断有各个国家地区的科学研究提供了 mRNA 疫苗在真实世界的保护率,同时也给科学家提供了关于变异株的流行情况和免疫逃逸的信息。
1.1 辉瑞/BioNTech mRNA 疫苗(BNT162b2)以色列-真实世界有效性研究
2021 年 4 月 15 日,一篇关于 BNT162b2 在真实世界有效率的文献发表在新英格兰医学杂志(NEJM) 上。文中数据来自于以色列最大的医疗服务组织之一 Clalit Health Services (CHS),CHS 会员约 470 万人, 约占以色列总人口的 53%。样本人群为 16 岁以上,此前未有新冠感染记录的 CHS 会员。由于年龄、 性别、生活地区、环境、身体状况、疾病史等众多因素都有可能显著影响感染率,每 1 位疫苗接种 者都有 1 位未接种者作为对照。为尽量减少干扰,居住地不明者、医疗机构工作者及密接者、疗养 院居住者、居家者被排除在样本人群外。最终,接种者和未接种者人群数量分别为 596618 人。观察 期为 2020 年 12 月 20 日至 2021 年 2 月 1 日。记录数据分为三组:第一剂接种后 14-20 天、第一剂接种 后 21-27 天和第二季接种后 7 天。文献追踪了 5 个数据:记录感染(documented infection)、有症状感 染(symptomatic infection)、住院(hospitalization)、重症(severe illness)、死亡(death)。


III 期临床数据显示 mRNA 疫苗对新冠病毒的保护率高达 94%以上,国药传统灭活疫苗的保护率虽 远远高于 WHO 和 FDA 建议标准的 50%,但仍与 mRNA 疫苗差距明显。同时,mRNA 疫苗对 65 岁 及以上的老年群体的保护作用也非常可观:BNT162b2 对 64 岁以上群体的保护率为 94.7%,仅比 16-64 岁群体数据低 0.4%。Moderna 的 mRNA1273 对 64 岁以上人群的保护率为 86.4%,甚至高于灭 活疫苗的整体保护率。(报告来源:未来智库)
真实世界数据应证 mRNA 疫苗高保护率,仍能有效应对变异株
随着 BNT162b2 和 mRNA1273 在全球多个国家开始接种,mRNA 疫苗真实世界保护率(Effectiveness)开 始揭开面纱。目前,BNT162b2 已在全球大范围接种。近期,不断有各个国家地区的科学研究提供了 mRNA 疫苗在真实世界的保护率,同时也给科学家提供了关于变异株的流行情况和免疫逃逸的信息。
1.1 辉瑞/BioNTech mRNA 疫苗(BNT162b2)以色列-真实世界有效性研究
2021 年 4 月 15 日,一篇关于 BNT162b2 在真实世界有效率的文献发表在新英格兰医学杂志(NEJM) 上。文中数据来自于以色列最大的医疗服务组织之一 Clalit Health Services (CHS),CHS 会员约 470 万人, 约占以色列总人口的 53%。样本人群为 16 岁以上,此前未有新冠感染记录的 CHS 会员。由于年龄、 性别、生活地区、环境、身体状况、疾病史等众多因素都有可能显著影响感染率,每 1 位疫苗接种 者都有 1 位未接种者作为对照。为尽量减少干扰,居住地不明者、医疗机构工作者及密接者、疗养 院居住者、居家者被排除在样本人群外。最终,接种者和未接种者人群数量分别为 596618 人。观察 期为 2020 年 12 月 20 日至 2021 年 2 月 1 日。记录数据分为三组:第一剂接种后 14-20 天、第一剂接种 后 21-27 天和第二季接种后 7 天。文献追踪了 5 个数据:记录感染(documented infection)、有症状感 染(symptomatic infection)、住院(hospitalization)、重症(severe illness)、死亡(death)。
接种第一剂后 14-20 天各项保护率数据如下:记录感染保护率 46%、有症状感染保护率 57%、住院保 护率 74%、重症保护率 62%、死亡保护率 72%。接种第一剂后 21-27 天各项保护率数据如下:记录感染保护率 60%、有症状感染保护率 66%、住院保 护率 78%、重症保护率 80%、死亡保护率 84%。接种第二剂 7 天后各项保护率数据如下:记录感染保护率 92%、有症状感染保护率 94%、住院保护率 87%、重症保护率 92%。因没有死亡病例,因此此数据无法进行数学计算。
文献指出,有症状感染保护率从第一剂接种后 12 天开始逐渐显著。在完成 2 剂接种 7 天后,保护率 约 94%,达到了非常理想的水平。从以上数据来看,接种 1 剂后,疫苗便能提供较好的预防中症和 重症的效果。对于无症状或轻度症状感染,接种 2 剂疫苗后的保护率有显著提升,真实世界数据与 此前临床 III 期数据接近,均接近 90%。以上数据均来源于以色列的真实世界数据,BNT162b2 在本次真实世界的考验中表现优秀,并且展现 两大特点:一是接种一剂后便能大幅降低中、重症的发生概率;二是完全接种后,对无症状或轻症 的保护率也高达 90%以上,可以有效阻碍或减缓新冠病毒的传播。
由于保护率来源于真实世界,因此疫苗效力面临着复杂的变异株型的考验。本次数据收集期间,在 以色列流行的新冠病毒株型主要为 B.1.1.7,即最早发现于英国的 Alpha 变异株,Alpha 变异株引起的感 染约占 80%。因此,本次实验应证了 BNT162b2 对于 B.1.1.7 变异株仍具有较高效力。
1.2 辉瑞/BioNTech mRNA 疫苗(BNT162b2)卡塔尔-真实世界有效性研究
2021 年 7 月 8 日,新英格兰医学杂志刊登了一篇关于 BNT162b2 在卡塔尔的真实世界数据报告。从 2020 年 12 月 21 日至 2021 年 3 月 31 日,卡塔尔共有 385853 人接种了至少 1 剂 BNT162b2,265410 人完成了 2 剂接种。根据病毒基因测序,2021年 2月 23日至 3 月 18日期间,在卡塔尔发生的新冠感染中,有 50.0%由 B.1.351 变异株引起,44.5%由 B.1.1.7 变异株引起。
文中数据反映了疫苗在真实世界面对这两种变异株的有效 保护率。同时文献将疫苗针对两种变异株型分别进行了数据分析。本次保护率数据分为感染保护率和重症保护率。感染的判断标准定义为 PCR 阳性,重症的判断标准 与 WHO 标准一致。本次检测、接种、感染等数据均取于 2021 年 2 月 1 日-3 月 31 日之间。若以 2020 年 12 月 21 日卡塔尔 大规模接种疫苗开始计算,此真实数据反映了完成两剂常规接种后 2-3 月疫苗所提供的保护率。
根据本次卡塔尔的真实世界数据,接种 2 剂 BNT162b2 后,对 B.1.1.7(Alpha)的感染保护率为 89.5%, 重症保护率为 100%。对于由任何一种新冠病毒株型引起的感染,BNT162b2 能够提供 97.4%的重症保 护率;对 B.1.351(Beta)的感染保护率为 75.0%,重症保护率为 100%。由以上数据可以看出,完整接种完 BNT162b2 后,疫苗能够对任何新冠病毒株型引起的重症感染,提 供极高的重症保护率。BNT162b2 对新冠病毒感染的保护率由所下滑,III 期临床数据显示的感染保护 率高达 94%,而本次真实世界数据显示疫苗对 B.1.1.7(Alpha)或 B.1.351(Beta)的感染保护率均略低 于 90%。不过疫苗仍旧提供了理想的感染保护率。
需要注意文献正文采用了检测阴性病例-控制(test-negative case-control study)的方法计算有效性,即:疫苗有效性 = 1 - (感染者中接种过疫苗*未感染者中未接种疫苗)/(未感染者中接种过疫苗*感染者 中未接种疫苗),因此,部分保护率与 BNT162b2 的 III 期数据有所出入。文献补充材料中也运用了 III 期的保护率计算公式:疫苗有效性 = 1 -(接种者感染率)/(抗体阴性者 感染率)。完成接种 2 剂新冠疫苗 14 天后,以此计算的真实世界保护率中,针对 B.1.1.7 的感染保护 率为 87.0%,针对 B.1.351 的感染保护率为 72.1%,针对不明变异株的感染保护率为 69.0%。
1.3 辉瑞/BioNTech mRNA 疫苗(BNT162b2)卡塔尔-真实世界有效性研究
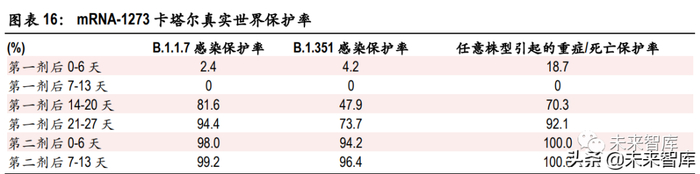
2021 年 7 月 9 日,Nature Medicine 刊登了一篇关于 mRNA-1273 在卡塔尔的真实世界数据报告。从 2020 年 12 月 28 日至 2021 年 5 月 10 日之间,卡塔尔共有 256037 人接种了至少 1 剂 mRNA-1273 新冠疫苗, 181304 人完成了 2 剂 mRNA-1273 的接种。根据接种记录,所有接种者接种第一剂的时间中位数是 2021 年 4 月 5 日,接种第二剂的时间中位数是 2021 年 4 月 29 日。
接种后不同时段,疫苗提供的保护率差异较为明显。只接种一剂与完成完整的两剂保护率差异尤其 明显。接种第一剂后 2 周内,疫苗提供的保护率几乎可忽略,原因在于首次感染后需要 1-2 周左右的 时间训练免疫系统形成特异免疫。接种第一剂后第 3 周开始,保护率呈现明显的上升趋势,直到 90% 左右的保护率水平。接种第二剂后,保护率进一步提升至 95%左右水平,重症以上保护率为 100%。从变异株型来看,疫苗针对 B.1.1.7(Alpha 变异株,英国)的保护率高于对 B.1.351(Beta 变异株,南 非)的保护率。此前,多个实验及真实世界数据显示 Beta 变异株能够较为明显地降低抗体的中和能 力。此真实世界数据展示的趋势与此相吻合。
1.4 辉瑞/BioNTech mRNA 疫苗(BNT162b2)及阿斯利康/牛津大学病毒载体疫苗(ChAdOx1) 英格兰-真实世界有效性研究
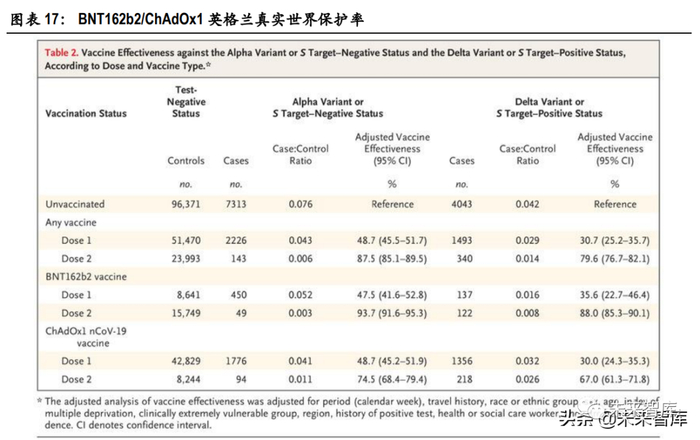
2021 年 7 月 21 日,一项由英格兰公共卫生部主导的关于 BNT162b2 和 ChAdOx1 nCoV-19(阿斯利康腺 病毒载体新冠疫苗)抵抗 Delta 变异株的真实世界研究,并在新英格兰医学杂志上刊登了数据和分析。研究采用了检测阴性病例-控制(test-negative case-control study)方法。疫苗接种率数据采集于 2021 年 5 月 17 日,疫苗接种情况分为,1. 接种第一剂 21 天后且尚未接种第二剂;2. 接种第二剂 14 天后。实验结果显示,接种 1 剂 BNT162b2 针对 Alpha 变异株的保护率为 47.5%(95%CI:41.6%-52.8%),针 对 Delta 变异株的保护率为 35.6%(95%CI:22.7%-46.4%)。
接种 2 剂 BNT162b2 针对 Alpha 变异株的保 护率为 93.7%(95%CI:91.6%-95.3%),针对 Delta 变异株的保护率为 88.0%(95%CI:85.3%-90.1%)。以上数据清晰显示,相较于不接种疫苗或只接种 1 剂疫苗,完整接种 2 剂疫苗后,疫苗提供的保护 率显著提高,并且对 Alpha 和 Delta 两种强传染性变异株的保护率均达到了约 90%的水平。
1.5 Moderna mRNA 疫苗(mRNA-1273)真实世界有效性研究
2021 年 9 月 15 日,Moderna 在其新闻发布会上更新了其 mRNA 路线新冠疫苗 mRNA-1273 的数据表 现。根据 Kaiser Permanente 在南加州的数据,样本人群为 352878 位接种了 2 剂次 mRNA-1273 的接 种者和相同数量的未接种疫苗者。疫苗接种时间为 2020 年 12 月 18 日至 2021 年 3 月 31 日,数据 收集时间截止于 2021 年 6 月 30 日。接种者与随机选择的非接种者根据年龄、性别、种族等属性 一一对应形成对照组。最终结果显示,mRNA-1273 疫苗有效性如下:对确诊新冠的保护率为 87.4%,对新冠引起的住院的保 护率为 95.8%。同时,在接种者感染病例中:Delta 引起了其中 47.1%的感染案例,Alpha 21.4%,Gamma 11.4%,Epsilon 4.3%,Iota 4.3%。在非接种者感染病例中:Alpha 引起了其中 41.2%的感染案例,Epsilon 18.2%,Delta 11.0%, Gamma 8.6%。
4 MRNA新冠疫苗加强针–三个问题
在讨论加强针时,我们面对三个核心问题,首先,我们需不需要加强针?如果答案是肯定的话,我们在 什么时间节点需要加强针?加强针以何种方式接种?以下内容对这三个问题进行了探究和分析。
我们需不需要加强针?
第一个问题,我们需不需要加强针?在上篇报告中,我们根据疫苗的保护周期以及病毒变异做出了 肯定的预测。从目前形势来看,这一预测正逐步兑现。
疫苗效力随时间递减
任何技术路径的疫苗产生的抗体水平都会随时间推移而递减,导致人体在遭到病毒侵袭时反应速度 下降,造成核酸检测结果阳性,因此疫苗提供的感染保护率也会逐渐下滑。不同技术路线的疫苗效 力衰减的时间有所区别。不同疫苗初始诱导的抗体滴度不同,因此抗体下降速度不同。因为抗体滴度与保护率呈现明显的正 相关关系,因此,高保护率常常伴随高抗体滴度。初始保护率越高,有效保护时间越长。因此,具 有高保护率的 BioNTech 和 Moderna 的 mRNA 疫苗应同时具有最持久的保护力。其他疫苗的保护周期应 短于这两款疫苗。根据目前数据,疫苗对抗感染的保护周期应在半年左右。
0 月 4 日-7 日,国际卫生组织 WHO 的 SAGE 专家会纪要中专门提到:接种国药或科兴灭活新冠疫 苗的 60 岁及以上人群,应(should)及时接种第三针,原则上推荐使用同源疫苗,但也可根据供 需情况考虑非同源的疫苗。而此前 WHO 多次表达反对过早开始加强针接种,尤其是在全球疫苗 缺口巨大,大量发展中国家需求远未满足的情况下。WHO 仅仅建议(recommended)中重度免疫 缺陷者接种加强针。


1.4 辉瑞/BioNTech mRNA 疫苗(BNT162b2)及阿斯利康/牛津大学病毒载体疫苗(ChAdOx1) 英格兰-真实世界有效性研究
2021 年 7 月 21 日,一项由英格兰公共卫生部主导的关于 BNT162b2 和 ChAdOx1 nCoV-19(阿斯利康腺 病毒载体新冠疫苗)抵抗 Delta 变异株的真实世界研究,并在新英格兰医学杂志上刊登了数据和分析。研究采用了检测阴性病例-控制(test-negative case-control study)方法。疫苗接种率数据采集于 2021 年 5 月 17 日,疫苗接种情况分为,1. 接种第一剂 21 天后且尚未接种第二剂;2. 接种第二剂 14 天后。实验结果显示,接种 1 剂 BNT162b2 针对 Alpha 变异株的保护率为 47.5%(95%CI:41.6%-52.8%),针 对 Delta 变异株的保护率为 35.6%(95%CI:22.7%-46.4%)。
接种 2 剂 BNT162b2 针对 Alpha 变异株的保 护率为 93.7%(95%CI:91.6%-95.3%),针对 Delta 变异株的保护率为 88.0%(95%CI:85.3%-90.1%)。以上数据清晰显示,相较于不接种疫苗或只接种 1 剂疫苗,完整接种 2 剂疫苗后,疫苗提供的保护 率显著提高,并且对 Alpha 和 Delta 两种强传染性变异株的保护率均达到了约 90%的水平。

1.5 Moderna mRNA 疫苗(mRNA-1273)真实世界有效性研究
2021 年 9 月 15 日,Moderna 在其新闻发布会上更新了其 mRNA 路线新冠疫苗 mRNA-1273 的数据表 现。根据 Kaiser Permanente 在南加州的数据,样本人群为 352878 位接种了 2 剂次 mRNA-1273 的接 种者和相同数量的未接种疫苗者。疫苗接种时间为 2020 年 12 月 18 日至 2021 年 3 月 31 日,数据 收集时间截止于 2021 年 6 月 30 日。接种者与随机选择的非接种者根据年龄、性别、种族等属性 一一对应形成对照组。最终结果显示,mRNA-1273 疫苗有效性如下:对确诊新冠的保护率为 87.4%,对新冠引起的住院的保 护率为 95.8%。同时,在接种者感染病例中:Delta 引起了其中 47.1%的感染案例,Alpha 21.4%,Gamma 11.4%,Epsilon 4.3%,Iota 4.3%。在非接种者感染病例中:Alpha 引起了其中 41.2%的感染案例,Epsilon 18.2%,Delta 11.0%, Gamma 8.6%。
4 MRNA新冠疫苗加强针–三个问题
在讨论加强针时,我们面对三个核心问题,首先,我们需不需要加强针?如果答案是肯定的话,我们在 什么时间节点需要加强针?加强针以何种方式接种?以下内容对这三个问题进行了探究和分析。
我们需不需要加强针?
第一个问题,我们需不需要加强针?在上篇报告中,我们根据疫苗的保护周期以及病毒变异做出了 肯定的预测。从目前形势来看,这一预测正逐步兑现。
疫苗效力随时间递减
任何技术路径的疫苗产生的抗体水平都会随时间推移而递减,导致人体在遭到病毒侵袭时反应速度 下降,造成核酸检测结果阳性,因此疫苗提供的感染保护率也会逐渐下滑。不同技术路线的疫苗效 力衰减的时间有所区别。不同疫苗初始诱导的抗体滴度不同,因此抗体下降速度不同。因为抗体滴度与保护率呈现明显的正 相关关系,因此,高保护率常常伴随高抗体滴度。初始保护率越高,有效保护时间越长。因此,具 有高保护率的 BioNTech 和 Moderna 的 mRNA 疫苗应同时具有最持久的保护力。其他疫苗的保护周期应 短于这两款疫苗。根据目前数据,疫苗对抗感染的保护周期应在半年左右。
0 月 4 日-7 日,国际卫生组织 WHO 的 SAGE 专家会纪要中专门提到:接种国药或科兴灭活新冠疫 苗的 60 岁及以上人群,应(should)及时接种第三针,原则上推荐使用同源疫苗,但也可根据供 需情况考虑非同源的疫苗。而此前 WHO 多次表达反对过早开始加强针接种,尤其是在全球疫苗 缺口巨大,大量发展中国家需求远未满足的情况下。WHO 仅仅建议(recommended)中重度免疫 缺陷者接种加强针。
变异株对疫苗效力的削弱
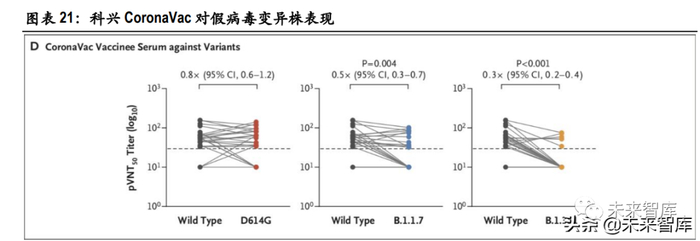
随着疫情的大肆流行,病毒开始出现多种变异。变异株的出现对于已有的新冠疫苗提出了挑战。由 于国内接种的国药、科兴疫苗均是以第一代野生型新冠病毒为基础,因此,诱导的免疫细胞的识别 对象也是第一代野生型病毒。变异株有可能无法被识别,造成疫苗效力削弱。以科兴疫苗在一次假病毒试验的数据为例,科兴新冠疫苗面对 D614G 单位点突变使疫苗诱导的 50% 假病毒中和抗体滴度下降至面对野生型病毒(WT)的 0.8 倍,面对 B.1.1.7(Alpha)时降至 WT 的 0.5 倍,面对 B.1.351(Beta)时降至 WT 的 0.3 倍,且有多个样本中检测不到中和抗体。因此,在考虑到 变异株的情况下,疫苗能够提供的保护率或许下降得更快。
行政防疫手段终将放松
此次疫情中,国内疫情控制表现非常优异。除 2020 年初刚刚爆发时出现了大规模感染,2020 年 3 月 以后,每月新增确诊均在 3000 例以下。对于一个 14 亿人口的大国来说,此次疫情控制充分展现了我 国体制在应对突发性公共事件时的反应力和执行力。然而,紧缩的政策是有代价的,国际交流、国 际贸易等受到冲击,相关经济较为萎靡。限制国际交流短期能够保护国民不受疫情影响,但似乎不 是长久之计。因此,可以预见未来重新开放国门与国际接轨确定性高。届时,一个由高效疫苗筑起 的免疫屏障非常必要。目前来看,初代灭活疫苗或难以胜任这一角色。
以色列加强针广泛接种后,疫情再次得到压制
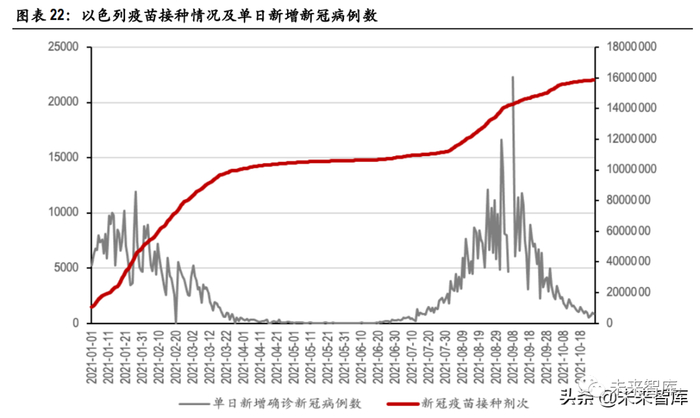
以色列已率先开展了大规模的加强针接种。2021 年以来,以色列经历了 2 波疫情冲击,但是当疫苗 接种数增加后,2 轮疫情均得到了明显压制。2021 年年初,以色列单日新增新冠病例长期处于 6000 例以上,1 月份平均每日新增病例约 7100 例。与此同时,以色列开始了大规模的疫苗接种,截至 1 月底,共接种疫苗 495.8 万剂。疫苗接种在 2 月 份便初显成效,2 月份平均每日新增 4727.6 例,较 1 月份有明显下滑。随着疫苗接种的不断提升,以 色列疫情得到了有效控制。
截至 4 月 30 日,以色列共接种 1046.8 万剂新冠疫苗,5 月份时以色列每 日新增病例数已下降至两位数。以色列的第二轮疫情开始于 2021 年 7 月,与第一轮疫苗接种开始时间间隔 6 个月。此后,每日新增 病例数于 8-9 月达到第二轮疫情的区域高峰,其中 9 月份平均每日新增病例数为 7710,并有数日单日 新增超过 10000 例。以色列在 8 月份加快了加强针的接种,8 月以色列共接种新冠疫苗 257.3 万剂, 其中,226.4 万剂为加强针。
截至 9 月底,以色列共接种新冠疫苗 1518.76 剂,其中包括 341.5 万剂加 强针。随着加强针的铺开,当地疫情再次出现明显地好转,10 月份单日新增病例数已由万例级别逐 渐下降至三位数水平。两轮疫情爆发初期,以色列能够及时地提升疫苗接种数。随着疫苗接种的提升, 单日新增病例数能够在约 1 个月后出现明显的下滑,与疫苗的生效时间相呼应,证明了疫苗对于疫 情控制的有效性。此外,第二轮疫情爆发的时间与第一轮疫苗有效期的结束时间几乎吻合,对于评 估疫苗有效期的长短起到一定作用,为未来疫情疫苗的走势提供了预测依据。
什么时间节点?
在肯定了加强针的必要性后,我们需要预测开展加强针接种的时间节点。时间节点与疫苗的保护周 期密切相关。
卡塔尔-BNT162b2 疫苗效力下滑趋势
卡塔尔一项研究显示,BNT162b2 的感染保护率在接种第二剂 1 个月后便开始逐步下降,4 个月后感染 保护率仅为 51.7%,仅与科兴灭活新冠疫苗的 III 期数据相当;5 个月后,BNT162b2 保护率降至 22.5%, 随后维持在类似水平。令人欣慰的是,BNT162b2 的住院及死亡保护率较为稳定,自完成完整的 2 剂接种后的半年内,保护 率基本维持在 95%左右。


行政防疫手段终将放松
此次疫情中,国内疫情控制表现非常优异。除 2020 年初刚刚爆发时出现了大规模感染,2020 年 3 月 以后,每月新增确诊均在 3000 例以下。对于一个 14 亿人口的大国来说,此次疫情控制充分展现了我 国体制在应对突发性公共事件时的反应力和执行力。然而,紧缩的政策是有代价的,国际交流、国 际贸易等受到冲击,相关经济较为萎靡。限制国际交流短期能够保护国民不受疫情影响,但似乎不 是长久之计。因此,可以预见未来重新开放国门与国际接轨确定性高。届时,一个由高效疫苗筑起 的免疫屏障非常必要。目前来看,初代灭活疫苗或难以胜任这一角色。
以色列加强针广泛接种后,疫情再次得到压制
以色列已率先开展了大规模的加强针接种。2021 年以来,以色列经历了 2 波疫情冲击,但是当疫苗 接种数增加后,2 轮疫情均得到了明显压制。2021 年年初,以色列单日新增新冠病例长期处于 6000 例以上,1 月份平均每日新增病例约 7100 例。与此同时,以色列开始了大规模的疫苗接种,截至 1 月底,共接种疫苗 495.8 万剂。疫苗接种在 2 月 份便初显成效,2 月份平均每日新增 4727.6 例,较 1 月份有明显下滑。随着疫苗接种的不断提升,以 色列疫情得到了有效控制。
截至 4 月 30 日,以色列共接种 1046.8 万剂新冠疫苗,5 月份时以色列每 日新增病例数已下降至两位数。以色列的第二轮疫情开始于 2021 年 7 月,与第一轮疫苗接种开始时间间隔 6 个月。此后,每日新增 病例数于 8-9 月达到第二轮疫情的区域高峰,其中 9 月份平均每日新增病例数为 7710,并有数日单日 新增超过 10000 例。以色列在 8 月份加快了加强针的接种,8 月以色列共接种新冠疫苗 257.3 万剂, 其中,226.4 万剂为加强针。
截至 9 月底,以色列共接种新冠疫苗 1518.76 剂,其中包括 341.5 万剂加 强针。随着加强针的铺开,当地疫情再次出现明显地好转,10 月份单日新增病例数已由万例级别逐 渐下降至三位数水平。两轮疫情爆发初期,以色列能够及时地提升疫苗接种数。随着疫苗接种的提升, 单日新增病例数能够在约 1 个月后出现明显的下滑,与疫苗的生效时间相呼应,证明了疫苗对于疫 情控制的有效性。此外,第二轮疫情爆发的时间与第一轮疫苗有效期的结束时间几乎吻合,对于评 估疫苗有效期的长短起到一定作用,为未来疫情疫苗的走势提供了预测依据。

什么时间节点?
在肯定了加强针的必要性后,我们需要预测开展加强针接种的时间节点。时间节点与疫苗的保护周 期密切相关。
卡塔尔-BNT162b2 疫苗效力下滑趋势
卡塔尔一项研究显示,BNT162b2 的感染保护率在接种第二剂 1 个月后便开始逐步下降,4 个月后感染 保护率仅为 51.7%,仅与科兴灭活新冠疫苗的 III 期数据相当;5 个月后,BNT162b2 保护率降至 22.5%, 随后维持在类似水平。令人欣慰的是,BNT162b2 的住院及死亡保护率较为稳定,自完成完整的 2 剂接种后的半年内,保护 率基本维持在 95%左右。
美国-BNT162b2 疫苗效力下滑趋势
另一项在美国开展的研究得到了类似的结果。结果显示,完全接种 BNT162b2 疫苗 1 个月后,疫苗感 染保护率为 88%;5 个月后,感染保护率仅剩 47%。针对 65 岁以上老年群体,疫苗展现了相似的保 护率:完全接种 1 个月后,感染保护率为 80%;5 个月后,感染保护率降至 43%。不过,BNT162b2 的 重症(住院)保护率仍旧稳定地维持在接近 90%。由此可推测,第一轮 mRNA 疫苗的接种程序对抗感染仅有半年左右的保护时长。
加强针接种时点为完成免疫程序后 6 个月
由以上两个案例可以看到,mRNA 疫苗在完成接种程序后半年,保护率逐渐降低至 50%以下,而其他 疫苗的保护周期应短于 6 个月,因此理论上完成主要免疫程序后 6 个月便进入接种加强针的合适时 段。但是,由于目前新冠疫苗仍处于紧缺状态,WHO 呼吁应尽早提高完成第一轮主要免疫程序的人 数,这一优先级高于加强针。此外,过早接种加强针对中和抗体的刺激并不可观,经济效率较低。因此,理想的接种时点应在完成主要免疫程序 6 个月后。此外,加强针对接种间隔要求并不严苛, 完成主要免疫程序后间隔 6 个月以上接种加强针仍旧能够有很好的巩固效果。
根据国内新冠疫苗接种情况,5 月中旬至 8 月底,疫苗接种剂次较高。4 月接种剂次为 1.44 亿,5 月 4.12 亿,6 月 5.82 亿,7 月 4.05 亿,8 月 4.07 亿,9 月 1.36 亿。4-9 月共计接种 20.86 亿剂次。加强针开 始时段为对应月份的 6 个月之后,据此预测,2021 年 11 月下旬至 2022 年 5 月将是加强针放量的时间 段。加强针为每人 1 剂次,对应需求量为 10.43 亿剂次。
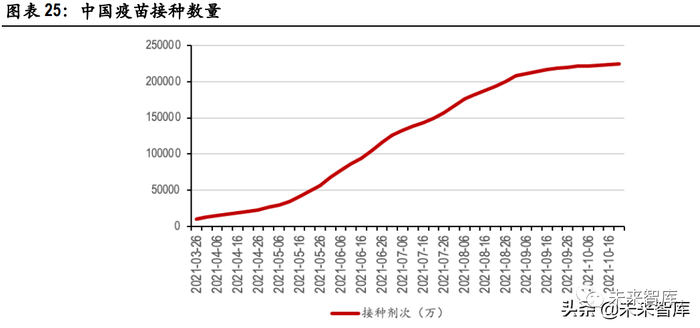
根据卫健委公告,截至 6 月 10 日,完成主要免疫程序的人数约为 2.233 亿人。截至 9 月 6 日,完成主 要免疫程序的人数约为 9.697 亿人。截至 10 月 23 日,完成主要免疫程序人数为 10.676 亿人。由于疫 苗供给紧张,且加强针与主要免疫程序之间的间隔周期可根据实际情况延长,因此,我们假设加强 针的接种时间为免疫程序完成后 6-8 个月。其余假设条件如下:加强针均为 1 剂次;所有已完成主要 免疫程序的公民均进行加强。由此可预测 2022 年 2 月前,加强针市场需求对应 2.233 亿剂次;2022 年 2-5 月,加强针需求约为 7.464 亿剂次;2022 年 5-7 月,加强针需求接近 1 亿剂次。(报告来源:未来智库)
由于以上预测基于所有适应人群均接受加强针的假设,实际需求可能小于测算结果。导致需求不及 预期的情况包括但不仅限于:1. 全球疫情得到控制,新冠成为地方性流行病:对加强针的需求影响 取决于疫情控制情况以及时点。根据目前海外疫情的发展趋势以及全球疫苗的接种率,全球范围内 的疫情有效控制出现的时机大概率晚于 2022 年 7 月份。2. 加强针为自愿接种:第二种情况取决于民 众对疫苗的信任程度以及依赖度,同时也受全球及全国疫情走势的影响。若疫情持续恶化,则无法 排除全民加强的可能性。
如何打?
在肯定了加强针的必要性,预测加强针接种时点后,如何加强针是接下来需要考虑的问题。美国批准加强针 mix-and-match 接种方案 美国 CDC 于 10 月 21 日发布了新闻公告,对加强针的建议进行了背书,目前适合的加强针接种人群 为 1. 65 岁及以上;2. 18 岁以上并长期进行照料工作的(live in long-term care settings);3. 18 岁以上并 患有一些基础疾病的(have underlying medical conditions)4. 18 岁以上并长期居住于或工作于高风险环 境的(live/work in high-risk settings)。CDC 表示加强针的接种遵循 mix-and-match 原则,即民众无需考虑此前接种的疫苗类型(除非曾出现 严重不良反应),可自行从在美获批的 3 种疫苗中选择,包括:辉瑞/BioNTech 的 BNT162b2,Moderna 的 mRNA-1273(50ug),强生的 Ad26.CoV2.S。根据主要免疫程序的疫苗类型,加强针的接种时间有所不同。若此前接种的是 mRNA 疫苗,即辉瑞 /BioNTech 或 Moderna 研制的疫苗,应在至少 6 个月之后接种加强针。若此前接种的是强生的病毒载体 疫苗,在至少 2 个月之后可接种加强针。CDC 表示,接种时点的不同主要出于疫苗有效性的考虑, 由于强生的病毒载体疫苗有效性低于另外两款 mRNA 疫苗,因此要求间隔时间更短。
多个国家政府已对加强针作出接种指引
包括比利时、法国、德国、匈牙利、爱尔兰、立陶宛、卢森堡、马耳他、斯洛文尼亚、瑞典、英国、 塞尔维亚等欧洲国家已批准加强针的施打。其中大部分政府表示,加强针将优先分配给具有免疫缺 陷而更易感染新冠病毒的人群。对普通人群的加强针接种计划需要继续评估,有可能将在未来放开。
Moderna:加强针势在必行,正同步推进 3 条加强针管线
Moderna 于 2021 年上半年业绩发布会上表示,公司经过评估认为疫情将在 Delta 变异等因素的催化下 进一步恶化,接种加强针或将在今年冬季成为一项必要的措施。Moderna 正在同步推进 3 条加强针的 研发方案探索。目前加强针接种时间设计在接种常规第二剂 6 个月后。第一种方案,继续采用原型 mRNA-1273 作为加强针。实验数据显示,接种后第 29 天,针对新冠病毒 原型的中和抗体几何平均滴度上升 16.7 倍。第二种方案,采用针对个别变异株的特异加强针,如针对 Beta 的 mRNA-1273.351,针对 Delta 的 mRNA-1273.617。实验数据显示,接种后第 15 天,针对新冠病毒原型的中和抗体几何平均滴度上升 11.1 倍。接种后第 29 天,中和抗体几何平均滴度上升 11.3 倍。第三种方案,采用多价平台(mRNA-1273.211,mRNA-1273.213)。实验数据显示,接种后第 15 天,针 对新冠病毒原型的中和抗体几何平均滴度上升 38.7 倍。接种后第 29 天,中和抗体几何平均滴度上升 46.4 倍。


根据卫健委公告,截至 6 月 10 日,完成主要免疫程序的人数约为 2.233 亿人。截至 9 月 6 日,完成主 要免疫程序的人数约为 9.697 亿人。截至 10 月 23 日,完成主要免疫程序人数为 10.676 亿人。由于疫 苗供给紧张,且加强针与主要免疫程序之间的间隔周期可根据实际情况延长,因此,我们假设加强 针的接种时间为免疫程序完成后 6-8 个月。其余假设条件如下:加强针均为 1 剂次;所有已完成主要 免疫程序的公民均进行加强。由此可预测 2022 年 2 月前,加强针市场需求对应 2.233 亿剂次;2022 年 2-5 月,加强针需求约为 7.464 亿剂次;2022 年 5-7 月,加强针需求接近 1 亿剂次。(报告来源:未来智库)
由于以上预测基于所有适应人群均接受加强针的假设,实际需求可能小于测算结果。导致需求不及 预期的情况包括但不仅限于:1. 全球疫情得到控制,新冠成为地方性流行病:对加强针的需求影响 取决于疫情控制情况以及时点。根据目前海外疫情的发展趋势以及全球疫苗的接种率,全球范围内 的疫情有效控制出现的时机大概率晚于 2022 年 7 月份。2. 加强针为自愿接种:第二种情况取决于民 众对疫苗的信任程度以及依赖度,同时也受全球及全国疫情走势的影响。若疫情持续恶化,则无法 排除全民加强的可能性。
如何打?
在肯定了加强针的必要性,预测加强针接种时点后,如何加强针是接下来需要考虑的问题。美国批准加强针 mix-and-match 接种方案 美国 CDC 于 10 月 21 日发布了新闻公告,对加强针的建议进行了背书,目前适合的加强针接种人群 为 1. 65 岁及以上;2. 18 岁以上并长期进行照料工作的(live in long-term care settings);3. 18 岁以上并 患有一些基础疾病的(have underlying medical conditions)4. 18 岁以上并长期居住于或工作于高风险环 境的(live/work in high-risk settings)。CDC 表示加强针的接种遵循 mix-and-match 原则,即民众无需考虑此前接种的疫苗类型(除非曾出现 严重不良反应),可自行从在美获批的 3 种疫苗中选择,包括:辉瑞/BioNTech 的 BNT162b2,Moderna 的 mRNA-1273(50ug),强生的 Ad26.CoV2.S。根据主要免疫程序的疫苗类型,加强针的接种时间有所不同。若此前接种的是 mRNA 疫苗,即辉瑞 /BioNTech 或 Moderna 研制的疫苗,应在至少 6 个月之后接种加强针。若此前接种的是强生的病毒载体 疫苗,在至少 2 个月之后可接种加强针。CDC 表示,接种时点的不同主要出于疫苗有效性的考虑, 由于强生的病毒载体疫苗有效性低于另外两款 mRNA 疫苗,因此要求间隔时间更短。
多个国家政府已对加强针作出接种指引
包括比利时、法国、德国、匈牙利、爱尔兰、立陶宛、卢森堡、马耳他、斯洛文尼亚、瑞典、英国、 塞尔维亚等欧洲国家已批准加强针的施打。其中大部分政府表示,加强针将优先分配给具有免疫缺 陷而更易感染新冠病毒的人群。对普通人群的加强针接种计划需要继续评估,有可能将在未来放开。
Moderna:加强针势在必行,正同步推进 3 条加强针管线
Moderna 于 2021 年上半年业绩发布会上表示,公司经过评估认为疫情将在 Delta 变异等因素的催化下 进一步恶化,接种加强针或将在今年冬季成为一项必要的措施。Moderna 正在同步推进 3 条加强针的 研发方案探索。目前加强针接种时间设计在接种常规第二剂 6 个月后。第一种方案,继续采用原型 mRNA-1273 作为加强针。实验数据显示,接种后第 29 天,针对新冠病毒 原型的中和抗体几何平均滴度上升 16.7 倍。第二种方案,采用针对个别变异株的特异加强针,如针对 Beta 的 mRNA-1273.351,针对 Delta 的 mRNA-1273.617。实验数据显示,接种后第 15 天,针对新冠病毒原型的中和抗体几何平均滴度上升 11.1 倍。接种后第 29 天,中和抗体几何平均滴度上升 11.3 倍。第三种方案,采用多价平台(mRNA-1273.211,mRNA-1273.213)。实验数据显示,接种后第 15 天,针 对新冠病毒原型的中和抗体几何平均滴度上升 38.7 倍。接种后第 29 天,中和抗体几何平均滴度上升 46.4 倍。
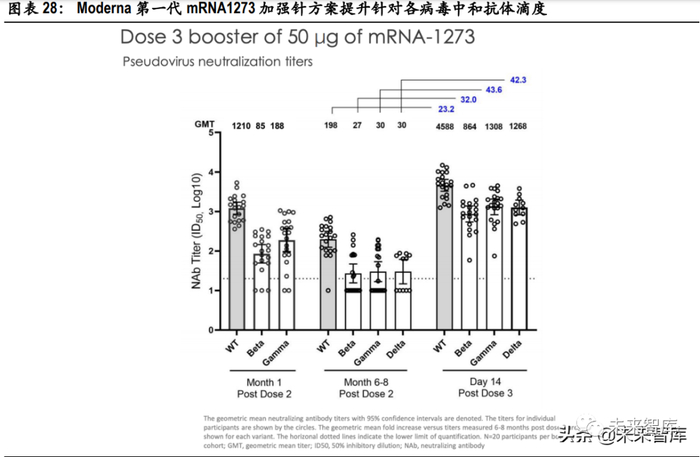
Moderna 同时也公布了加强针针对不同变异株的中和抗体几何滴度的变化。常规接 种 2 剂次后,经过 6-8 个月,对各变异株的中和抗体均有所下降,但仍能够被检测到。以常规接种完 成 6-8 月后留存的中和抗体滴度为基准,以 50ug 第一代 mRNA-1273 疫苗作为加强针,接种 14 天后, 得到以下数据:针对原型病毒(WT)的中和抗体滴度增加 23.2 倍,针对 Beta 变异株的中和抗体滴度 增加 32.0 倍,针对 Gamma 变异株的滴度增加 43.6 倍,针对 Delta 变异株的滴度增加 42.3 倍。
以主要免疫程序完成后 1 个月留存的中和抗体滴度为基准,加强针使针对野生型(WT)的中和抗体 滴度上升 3.79 倍,针对 Beta 变异株的中和抗体滴度上升 10.16 倍,针对 Gamma 变异株的中和抗体滴 度上升 6.96 倍。加强针对抗体滴度的提升在各年龄层均可观察到,在 65 岁及以上的老年群体中尤其明显。加强针的 安全性特征与前两针常规接种相似。
BNT162b2 加强针大幅提升抗体滴度
2021 年 7 月 28 日,辉瑞发布 21Q2 季度报告。报告披露,辉瑞和 BioNTech 正在推进 BNT162b2 新冠疫 苗第三剂加强针的临床试验。试验结果显示,在完成第二剂接种至少 6 个月后接种第三剂,加强针 能够非常明显地提升对新冠病毒各个变异株型的抗体滴度,同时维持与前两针一致的安全性。有效 性方面,针对野生型(第一代新冠病毒、原型)毒株,接种第三针后 1 个月所测得的中和抗体滴度 为接种第二针后 1 个月的 5.48 倍;针对南非变异株(B.1.351,Beta),接种第三针后 1 个月所测得的 中和抗体滴度为接种第二针后 1 个月的 15.01 倍;针对印度变异株(B.1.617.2,Delta),在青少年群 体中加强针能够提高中和抗体滴度 5 倍以上,老年群体提高 11 倍以上。
从以上数据可以看出加强针能够非常显著地提升接种者体内的抗体滴度,这表明此前 2 剂接种已高 效诱导了人体形成免疫记忆,因此 B 细胞能够在识别抗原后快速大量地扩增。2021 年 11 月 2 日,辉瑞三季度报告中提到加强针相对于仅完成主要免疫程序能够提供 95.6%的保护 率。即:1 - 接种加强针后(3 针)的感染概率 / 仅完成主要免疫(2 针)的感染概率 = 95.6%


BNT162b2 加强针大幅提升抗体滴度
2021 年 7 月 28 日,辉瑞发布 21Q2 季度报告。报告披露,辉瑞和 BioNTech 正在推进 BNT162b2 新冠疫 苗第三剂加强针的临床试验。试验结果显示,在完成第二剂接种至少 6 个月后接种第三剂,加强针 能够非常明显地提升对新冠病毒各个变异株型的抗体滴度,同时维持与前两针一致的安全性。有效 性方面,针对野生型(第一代新冠病毒、原型)毒株,接种第三针后 1 个月所测得的中和抗体滴度 为接种第二针后 1 个月的 5.48 倍;针对南非变异株(B.1.351,Beta),接种第三针后 1 个月所测得的 中和抗体滴度为接种第二针后 1 个月的 15.01 倍;针对印度变异株(B.1.617.2,Delta),在青少年群 体中加强针能够提高中和抗体滴度 5 倍以上,老年群体提高 11 倍以上。
从以上数据可以看出加强针能够非常显著地提升接种者体内的抗体滴度,这表明此前 2 剂接种已高 效诱导了人体形成免疫记忆,因此 B 细胞能够在识别抗原后快速大量地扩增。2021 年 11 月 2 日,辉瑞三季度报告中提到加强针相对于仅完成主要免疫程序能够提供 95.6%的保护 率。即:1 - 接种加强针后(3 针)的感染概率 / 仅完成主要免疫(2 针)的感染概率 = 95.6%
初步实验结果显示不同技术路径接种能够诱导高抗体滴度
2021 年 9 月,一篇由土耳其科学团队贡献的有关异源新冠疫苗的文章发表在 Journal of Medical Virology 上。实验初步探索了完成 2 剂次科兴灭活疫苗(CoronaVac)接种后,再以 BioNTech 的 mRNA 疫苗 (BNT162b2)作为加强针的临床效果,并与其他加强针方案进行了对比。本实验是为数不多的针对 灭活/mRNA 异源加强的实验,但实验本身局限于过小的样本量,因此参考价值有限,后续类似实验 需要长期关注。实验结果显示,接种 2 剂科兴灭活疫苗后,针对 S 蛋白的 IgG(IgG_S)滴度平均值为 1351.2 au/ml;接种 2 剂科兴灭活疫苗+1 剂科兴灭活加强针后,IgG_S 滴度平均值为 1215.8 au/ml;接种 2 剂科兴灭活 疫苗+1 剂 BNT162b2 后,IgG_S 滴度平均值为 31277.9 au/ml,远远高于 3 剂科兴灭活疫苗诱导的滴度。
有关国内加强针
由以上分析我们可以得到以下信息,国内加强针的主要接种时段为 2021 年 11 月-2022 年 5 月,若按 照全民接种进行假设,预计需求量约为 10 亿剂。2021 年 10 月开始的本轮疫情已经波及十几个省份,呈现多地零散爆发的特点。与此前预估的第一轮 新冠疫苗到期时间接近。由于加强针还未全面铺开,而大部分公民接种的第一轮疫苗的效力至今已 明显衰减,因此 2021 年 11 月至 2022 年 1 月期间将有可能出现疫苗保护期之间的断档期,加之冬季 到来,期间出现零散疫情的风险将增大。

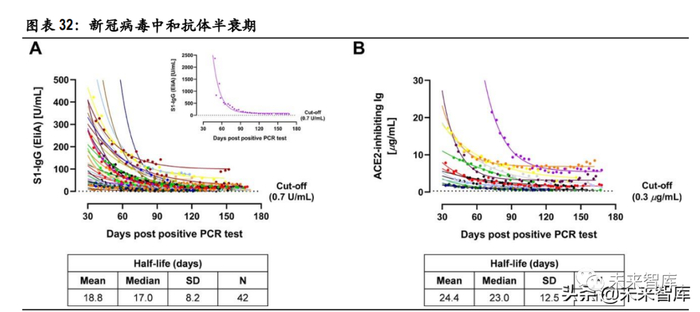
2021 年 10 月 30 日,中国疾控中心免疫规划首席专家王华庆先生在国务院联防联控机制新闻发布会 上表示,部分灭活疫苗接种完第三针满一个月后,和接种完第二针满一个月后相比,接种者抗体水 平提升约 5 倍。针对新冠病毒的中和抗体的平均半衰期为 20.4 天,其中 S1-IgG 的平均半衰期为 18.8 天,ACE2 抑制 Ig 的平均半衰期为 24.4 天。加强针诱导的额外 5 倍抗体滴度能够在主要免疫程序保护 期的基础上延长 2.32 个半衰期,约合 47.33 天。以乐观假设灭活疫苗中和抗体滴度能够维持在有效水 平以上约 6 个月,则加强针诱导的中和抗体滴度能够维持约 8 个月。
根据以上预测,第一轮加强针的保护周期可持续约 8-9 个月,而第一轮加强针的主要接种时点为 2021 年 11 月至 2022 年 5 月,则根据接种时间早晚,加强针可延长保护期至 2022 年 8 月至 2022 年底。届 时,若全球疫情仍未得到有效控制,则可能还需要第二轮加强针接种。在上一部分中,我们预测第一轮加强针的需求状况如下:2022 年 2 月前,加强针市场需求对应 2.23 亿剂次;2022 年 3-5 月,加强针需求约为 7.46 亿剂次;2022 年 5-7 月,加强针需求接近 1 亿剂次。第 二轮加强针的必要性和需求目前并不明朗,故不做预测。
5 MRNA疫苗生产要素:核心技术成本占比高,整体利润率可观
核心技术构成主要成本
2021 年 7 月 28 日,辉瑞发布 21Q2 季度报告。报告披露,辉瑞和 BioNTech 正在推进 BNT162b2 新冠疫 苗第三剂加强针的 1/2/3 期临床试验。试验结果显示,在完成第二剂接种至少 6 个月后接种第三剂, 加强针能够非常明显地提升中和抗体滴度,重新激活免疫记忆,并提高免疫力。
mRNA 疫苗的生产分为 4 大环节:DNA 质粒制备、体外转录及修饰、递送系统装载、灌装及检验检疫。生产过程中各 mRNA 疫苗厂商的核心技术主要集中在 TFF 微流控设备、阳离子脂质、以及修饰技术, 具有较高的技术和知识产权壁垒。根据已知信息,这一部分在成本构成中占比非常高。在此,我们 根据市场上已有产品信息对体外转录环节的成本构成进行初步估算。注意:由于厂商生产步骤可能 与此有差异,且大规模采购常有折价,因此,此估算结果与实际偏差可能较大。不过,此估算仍旧 对预测疫苗成本构成有参考价值。
此环节可分为 2 大部分:体外转录(IVT)合成 mRNA、对 mRNA 进行修饰。体外转录将已制备完成的 DNA 质粒转化为 mRNA 链。这一步骤中,传统反应酶类的成本占比较低, 而具有一定技术壁垒的反应物占据了主要的成本构成。常规反应物包括 RNA 聚合酶、ATP、GTP、UTP、 CTP、缓冲液、以及用于纯化过滤的制剂。而具有技术壁垒的反应物包括用于加帽的反应物、修饰碱 基(假尿嘧啶)。以下我们以 New England BioLabs(NEB)的产品为例,对此步骤中常规反应物和壁 垒反应物进行成本对比。由于大规模采购的价格与零售定价单位成本相差较大,因此此处我们不考 虑价格绝对值,而仅估算成本构成比例作为参考。
NEB 产品中,HiScribe® T7 High Yield RNA Synthesis Kit(E2040)用于转录合成 mRNA。每个 E2040 kit 中所含的反应物可满足 50 次反应,每次反应生产 180ug 的 RNA。即每个 kit 可用于生产 9000ug 的 RNA。根据 NEB 官网定价,E2040 单价为 232 美元。根据计算,则每生产 100ug mRNA,E2040 的成 本为 2.6 美元。对比相同厂家 NEB 的加帽产品,Vaccinia Capping System(M2080)和 mRNA Cap 2'-O-Methyltransferase (M0366)作为加帽过程成本预测的假设基础。M2080 的规格为 400/10000=0.04ml=40ul,可满足 40 次反 应的需求,每次反应可生成至多 10ug 加帽 mRNA。据此测算,每生产 100ug mRNA,需要 1/4 份 M2080。
根据 NEB 官网定价,一份 M2080 价格为 140 美金,则每生产 100ug 加帽 mRNA,M0366 构成的成本为 140/4=35 美金。M0366 的规格为 2000/50000=0.04ml=40ul,可满足 40 次反应的需求,每次反应可生成至 多 10ug 加帽 mRNA。据此测算,每生产 100ug mRNA,需要 1/4 份 M0366。根据 NEB 官网定价,一份 M0366 价格为 58 美金,则每生产 100ug 加帽 mRNA,M0366 构成的成本为 58/4=14.5 美金。加帽过程的 总成本为 35+14.5=49.5 美金。从以上估算可以看出,加帽成本是常规合成酶类成本的约 19 倍。虽然估算不完全准确,但可以显示 生产中高技术壁垒的反应制剂所占成本非常高。
现有 mRNA 疫苗毛利率约 90%
根据 Moderna(MRNA)10-Q 报告,公司在截至 2021 年 6 月 30 日的三个月内实现产品销售收入 42 亿 美元,收入来源于供给美国政府的约 1.26 亿剂新冠疫苗和供给其他政府的约 0.73 亿剂新冠疫苗。期 间,公司营业成本为 7.50 亿美元,占产品销售收入的 18%,包括第三方 royalties1.48 亿美元。截至 2021 年 6 月 30 日的六个月内实现营业收入 62 亿美元,产品销售收入 59 亿美元,收入来源于供给美国政 府的约 2.15 亿剂新冠疫苗和供给其他政府的约 0.87 亿剂新冠疫苗。期间,公司营业成本为 9.43 亿美 元,占产品销售收入的 16%,包括第三方 royalties2.32 亿美元。剔除第三方支出,营业成本为 7.11 亿 元,毛利率为 87.95%。此前 Moderna 的新冠疫苗定价约为 20 美元/剂,以此计算,每剂疫苗成本约为 2.41 美元,约合 15 元人民币。
6 重点公司分析
沃森生物
公司业绩简介
沃森生物成立于 2001 年,长期深耕疫苗领域,拥有丰富的产品管线,包括已上市的 13 价肺炎结合疫 苗和正处于临床阶段的 2 价 HPV 疫苗、9 价 HPV 疫苗、以及 mRNA 新冠疫苗。公司 2020 年实现营业收入 29.39 亿元,同比增长 162.13%;归母净利润 10.03 亿元,同比增长 606.60%。2021 年第一季度实现营业收入 4.34 亿元,同比增长 286.45%;归母净利润 3215.88 万元,同比增长 277.50%。
2021 年前三季度,公司实现营业收入 21.29 亿元,同比增长 35.90%;归属于上市公司股东的净利润 3.64 亿元,同比减少 16.33%;归属于上市公司股东的扣除非经常性损益的净利润 3.85 亿元,同比减 少 10.96%;经营活动现金净流量 2.65 亿元,同比增长 135.14%。公司 2021 年前三季度批签发量出现下滑,主要系百白破疫苗、ACYW135 多糖疫苗、23 价肺炎疫苗下 滑较为明显。公司新上市的重磅品种 13 价肺炎结合疫苗维持增长。预计在明年,新冠疫苗接种的挤 压有望消退,公司批签发量将会有所恢复。


5 MRNA疫苗生产要素:核心技术成本占比高,整体利润率可观
核心技术构成主要成本
2021 年 7 月 28 日,辉瑞发布 21Q2 季度报告。报告披露,辉瑞和 BioNTech 正在推进 BNT162b2 新冠疫 苗第三剂加强针的 1/2/3 期临床试验。试验结果显示,在完成第二剂接种至少 6 个月后接种第三剂, 加强针能够非常明显地提升中和抗体滴度,重新激活免疫记忆,并提高免疫力。
mRNA 疫苗的生产分为 4 大环节:DNA 质粒制备、体外转录及修饰、递送系统装载、灌装及检验检疫。生产过程中各 mRNA 疫苗厂商的核心技术主要集中在 TFF 微流控设备、阳离子脂质、以及修饰技术, 具有较高的技术和知识产权壁垒。根据已知信息,这一部分在成本构成中占比非常高。在此,我们 根据市场上已有产品信息对体外转录环节的成本构成进行初步估算。注意:由于厂商生产步骤可能 与此有差异,且大规模采购常有折价,因此,此估算结果与实际偏差可能较大。不过,此估算仍旧 对预测疫苗成本构成有参考价值。
此环节可分为 2 大部分:体外转录(IVT)合成 mRNA、对 mRNA 进行修饰。体外转录将已制备完成的 DNA 质粒转化为 mRNA 链。这一步骤中,传统反应酶类的成本占比较低, 而具有一定技术壁垒的反应物占据了主要的成本构成。常规反应物包括 RNA 聚合酶、ATP、GTP、UTP、 CTP、缓冲液、以及用于纯化过滤的制剂。而具有技术壁垒的反应物包括用于加帽的反应物、修饰碱 基(假尿嘧啶)。以下我们以 New England BioLabs(NEB)的产品为例,对此步骤中常规反应物和壁 垒反应物进行成本对比。由于大规模采购的价格与零售定价单位成本相差较大,因此此处我们不考 虑价格绝对值,而仅估算成本构成比例作为参考。
NEB 产品中,HiScribe® T7 High Yield RNA Synthesis Kit(E2040)用于转录合成 mRNA。每个 E2040 kit 中所含的反应物可满足 50 次反应,每次反应生产 180ug 的 RNA。即每个 kit 可用于生产 9000ug 的 RNA。根据 NEB 官网定价,E2040 单价为 232 美元。根据计算,则每生产 100ug mRNA,E2040 的成 本为 2.6 美元。对比相同厂家 NEB 的加帽产品,Vaccinia Capping System(M2080)和 mRNA Cap 2'-O-Methyltransferase (M0366)作为加帽过程成本预测的假设基础。M2080 的规格为 400/10000=0.04ml=40ul,可满足 40 次反 应的需求,每次反应可生成至多 10ug 加帽 mRNA。据此测算,每生产 100ug mRNA,需要 1/4 份 M2080。
根据 NEB 官网定价,一份 M2080 价格为 140 美金,则每生产 100ug 加帽 mRNA,M0366 构成的成本为 140/4=35 美金。M0366 的规格为 2000/50000=0.04ml=40ul,可满足 40 次反应的需求,每次反应可生成至 多 10ug 加帽 mRNA。据此测算,每生产 100ug mRNA,需要 1/4 份 M0366。根据 NEB 官网定价,一份 M0366 价格为 58 美金,则每生产 100ug 加帽 mRNA,M0366 构成的成本为 58/4=14.5 美金。加帽过程的 总成本为 35+14.5=49.5 美金。从以上估算可以看出,加帽成本是常规合成酶类成本的约 19 倍。虽然估算不完全准确,但可以显示 生产中高技术壁垒的反应制剂所占成本非常高。
现有 mRNA 疫苗毛利率约 90%
根据 Moderna(MRNA)10-Q 报告,公司在截至 2021 年 6 月 30 日的三个月内实现产品销售收入 42 亿 美元,收入来源于供给美国政府的约 1.26 亿剂新冠疫苗和供给其他政府的约 0.73 亿剂新冠疫苗。期 间,公司营业成本为 7.50 亿美元,占产品销售收入的 18%,包括第三方 royalties1.48 亿美元。截至 2021 年 6 月 30 日的六个月内实现营业收入 62 亿美元,产品销售收入 59 亿美元,收入来源于供给美国政 府的约 2.15 亿剂新冠疫苗和供给其他政府的约 0.87 亿剂新冠疫苗。期间,公司营业成本为 9.43 亿美 元,占产品销售收入的 16%,包括第三方 royalties2.32 亿美元。剔除第三方支出,营业成本为 7.11 亿 元,毛利率为 87.95%。此前 Moderna 的新冠疫苗定价约为 20 美元/剂,以此计算,每剂疫苗成本约为 2.41 美元,约合 15 元人民币。
6 重点公司分析
沃森生物
公司业绩简介
沃森生物成立于 2001 年,长期深耕疫苗领域,拥有丰富的产品管线,包括已上市的 13 价肺炎结合疫 苗和正处于临床阶段的 2 价 HPV 疫苗、9 价 HPV 疫苗、以及 mRNA 新冠疫苗。公司 2020 年实现营业收入 29.39 亿元,同比增长 162.13%;归母净利润 10.03 亿元,同比增长 606.60%。2021 年第一季度实现营业收入 4.34 亿元,同比增长 286.45%;归母净利润 3215.88 万元,同比增长 277.50%。
2021 年前三季度,公司实现营业收入 21.29 亿元,同比增长 35.90%;归属于上市公司股东的净利润 3.64 亿元,同比减少 16.33%;归属于上市公司股东的扣除非经常性损益的净利润 3.85 亿元,同比减 少 10.96%;经营活动现金净流量 2.65 亿元,同比增长 135.14%。公司 2021 年前三季度批签发量出现下滑,主要系百白破疫苗、ACYW135 多糖疫苗、23 价肺炎疫苗下 滑较为明显。公司新上市的重磅品种 13 价肺炎结合疫苗维持增长。预计在明年,新冠疫苗接种的挤 压有望消退,公司批签发量将会有所恢复。
加强针临床实验获批,潜在产业化进程迈出重要一步
11 月 8 日,科技部官网显示沃森生物与合作伙伴联合研发的 mRNA 新冠疫苗加强针临床 IIIb 期实验获 批。侧面预示目前疫苗的 III 期临床大概率表现良好。加强针实验目的为探究疫苗免疫原性及安全性, 因此大概率将以血清学指标作为主要研究目标。一般来说,血清学指标的数据收集时点为给药后 2 周及给药后 1 个月,所需时间仅为 1 个月左右。进度的不确定性主要来自于志愿者入组速度、数据 整理、以及审批流程。由于国内新冠疫苗市场最大的未摘果实便是加强针,因此本次实验获批是产 品潜在商业化迈出的重要一步。

RBD 作为标靶,对抗变异效果理想。
军科院秦成峰教授在 2021 中关村第二届全球科学与生命健康论坛上披露,公司与艾博生物、军科院 共同研发的新冠 mRNA 疫苗目前显示能够诱导 2 倍于康复者血清的中和抗体滴度,与此前 BioNTech 的另一候选疫苗 BNT162b1 表现接近。根据 BioNTech 的披露,接种第二针 7 天后,10ug 和 30ug 剂量的 BNT162b1 诱导的中和抗体滴度分别为康复者血清的 1.8 倍和 2.8 倍,诱导的与 RBD 结合的 IgG 为康复 者血清的 8 倍和 46.3 倍。
根据前文分析,采用 RBD 作为疫苗表达目标,可以较好地抵抗变异带来的疫苗效力削弱。秦成峰教 授表示,公司研发的 mRNA 新冠疫苗针对 Delta 变异株中和抗体滴度仅下降 1.5 倍,优于其他同类产 品。同时,该疫苗能够实现 2-8 摄氏度下的保存,6 个月存储后并未发现免疫原性的显著丧失,与国 外两款 mRNA 疫苗较为严苛的存储要求相比具有优势。较为宽松的存储条件能够提升疫苗的可及性, 对于财政紧张的发展中国家来说更具有吸引力。(报告来源:未来智库)
新冠 mRNA 疫苗海外临床陆续获批,海外市场潜力巨大。
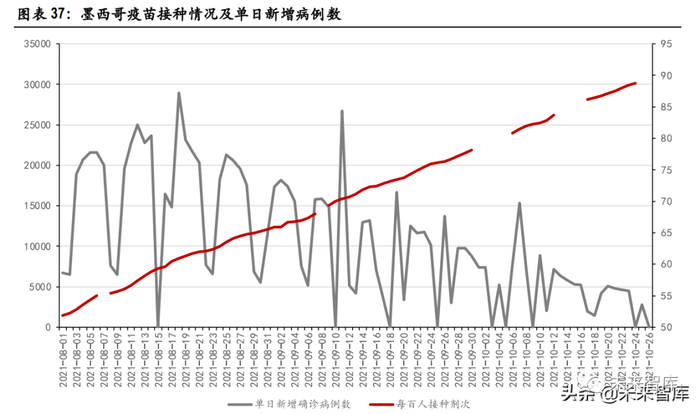
2021 年 9 月,公司新冠 mRNA 疫苗相继获得海外的开展临床 III 期实验批准。9 月 1 日,公司获得墨西 哥、印度尼西亚药监部门的批准;9 月 23 日,获得尼泊尔药监部门批准。9 月 14 日公司首批外派团 出发开展海外临床和技术转移。海外临床相继获批显示该疫苗的初期数据得到其他国家监管部门的 初步认可,且该产品具有开辟海外市场的潜力。目前,海外新冠疫苗需求仍旧巨大。墨西哥人口约 1.3 亿人。截至 2021 年 10 月 24 日,每百人接种剂次 88.76,有 53.78 人接种至少一剂, 有 41.34 人完成主要免疫。假设目标疫苗接种率为 70%,尚未开始主要免疫程序的人数约 2109 万,以 2 剂次/人计算,折合 4218 万剂疫苗的市场空间,且没有考虑潜在的加强针市场。


RBD 作为标靶,对抗变异效果理想。
军科院秦成峰教授在 2021 中关村第二届全球科学与生命健康论坛上披露,公司与艾博生物、军科院 共同研发的新冠 mRNA 疫苗目前显示能够诱导 2 倍于康复者血清的中和抗体滴度,与此前 BioNTech 的另一候选疫苗 BNT162b1 表现接近。根据 BioNTech 的披露,接种第二针 7 天后,10ug 和 30ug 剂量的 BNT162b1 诱导的中和抗体滴度分别为康复者血清的 1.8 倍和 2.8 倍,诱导的与 RBD 结合的 IgG 为康复 者血清的 8 倍和 46.3 倍。
根据前文分析,采用 RBD 作为疫苗表达目标,可以较好地抵抗变异带来的疫苗效力削弱。秦成峰教 授表示,公司研发的 mRNA 新冠疫苗针对 Delta 变异株中和抗体滴度仅下降 1.5 倍,优于其他同类产 品。同时,该疫苗能够实现 2-8 摄氏度下的保存,6 个月存储后并未发现免疫原性的显著丧失,与国 外两款 mRNA 疫苗较为严苛的存储要求相比具有优势。较为宽松的存储条件能够提升疫苗的可及性, 对于财政紧张的发展中国家来说更具有吸引力。(报告来源:未来智库)
新冠 mRNA 疫苗海外临床陆续获批,海外市场潜力巨大。
2021 年 9 月,公司新冠 mRNA 疫苗相继获得海外的开展临床 III 期实验批准。9 月 1 日,公司获得墨西 哥、印度尼西亚药监部门的批准;9 月 23 日,获得尼泊尔药监部门批准。9 月 14 日公司首批外派团 出发开展海外临床和技术转移。海外临床相继获批显示该疫苗的初期数据得到其他国家监管部门的 初步认可,且该产品具有开辟海外市场的潜力。目前,海外新冠疫苗需求仍旧巨大。墨西哥人口约 1.3 亿人。截至 2021 年 10 月 24 日,每百人接种剂次 88.76,有 53.78 人接种至少一剂, 有 41.34 人完成主要免疫。假设目标疫苗接种率为 70%,尚未开始主要免疫程序的人数约 2109 万,以 2 剂次/人计算,折合 4218 万剂疫苗的市场空间,且没有考虑潜在的加强针市场。
印度尼西亚人口约 2.76 亿人。截至 10 月 26 日,每百人接种剂次 66.39,有 41.38 人接种至少一剂,有 25.01 人完成主要免疫。假设目标疫苗接种率为 70%,尚未开始主要免疫程序的人数约 7899 万,以 2 剂次/人计算,折合 15800 万剂疫苗的市场空间,且没有考虑潜在的加强针市场。
尼泊尔人口总数 2967 万人。截至 10 月 19 日,每百人接种剂次 50.71,有 28.85 人接种至少一剂,有 21.86 人完成主要免疫。假设目标疫苗接种率为 70%,尚未开始主要免疫程序的人数约 1221 万,以 2 剂次/人计算,折合 2442 万剂疫苗的市场空间,且没有考虑潜在的加强针市场。
根据 BNT162b2 和 mRNA-1273 的疫苗和临床设计,2 剂次之间相隔 1 个月,主要数据的收集为第二剂 接种完成 1-2 周后。因此,假设以 9 月初为开针时点,则十月中旬开始主要数据收集。考虑到数据收 集和数据整理所需时间,可以期待在 2022 年初看到海外 III 期结果。
(本文仅供参考,不代表我们的任何投资建议。如需使用相关信息,请参阅报告原文。)

