
图片来源:图虫创意
对许多消费者而言,“医”这个字带有一种天然的公信力。尤其在功效性护肤赛道,不少品牌都青睐通过与皮肤科医生合作、邀请他们背书等方式在一定程度上证明自己的产品功效。
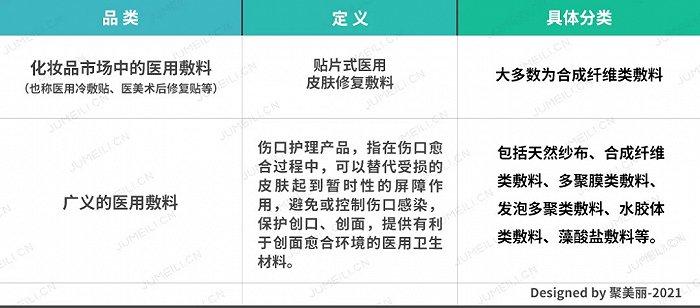
化妆品市场中,存在着一种自带“医用”宣传效果的品类——医用敷料,它也常被消费者称为医美术后修复贴或医美面膜。当我们提到医美面膜时,一般指的就是以敷尔佳、可复美、创福康等品牌为代表的医用冷敷贴。事实上,这类产品在广义的医用敷料范围中属于一个很小的分类,但不得不说,这两年医用敷料在化妆品行业中很火热。
(注:为方便叙述,下文将统称“医用敷料”,仅指化妆品市场中常见的医美术后修复贴)
据医疗健康媒体动脉网报道,2017年,小红书一篇包含20多个品牌的“医用面膜测评”的种草笔记带火了医用敷料。嗅觉敏锐的商家们迅速捕捉到了这一风口,在各大品牌方的营销资金支持下,医用敷料受到众多美妆博主的追捧,并迅速走进大众视野,掀起了一阵热潮。
一时间,市场上涌现了大量“械字号面膜”、“医美面膜”。2020年,国家药监局发文提示应警惕面膜消费陷阱,明确表示不存在“械字号面膜”这一说法。“械字号”指的是医疗器械产品的注册、备案号以“x械xx”开头,而没有一款“面膜”产品属于医疗器械。
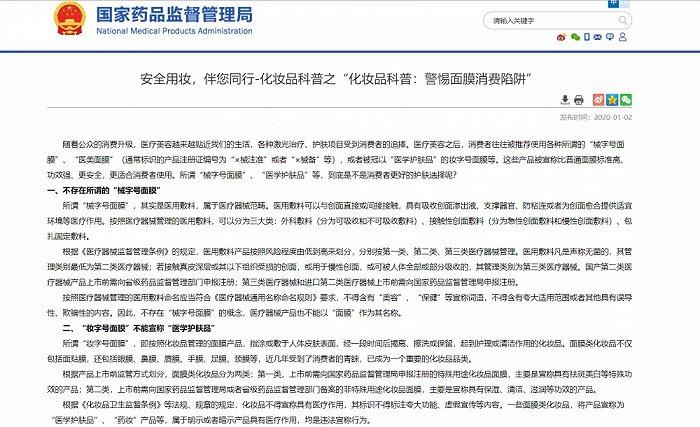
截图自国家药监局
虽然医美面膜已禁止宣称,但目前,小红书上关于“医美后面膜”、“医美修复面膜”的相关笔记仍然分别超过22w篇和18w篇,热度不减。
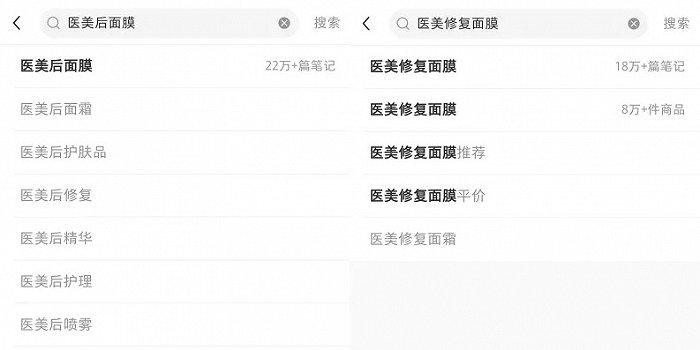
截图自小红书
那么,带上了“医用”、“医美”等宣称的医用敷料,与化妆品行业的普通面膜相比,除了在监管体系上的不同外,在原料、用途、技术等方面也会有很多不同吗?医用敷料真的有自己的技术壁垒吗?记者关于这个问题作了一些了解与调查。
5个维度对比医用敷料和普通面膜的差异
1)用途
“医用敷料在医院中目前主要针对两类患者使用,一类是需要在医美手术之后对受损皮肤进行修复和舒缓的患者,另一类是存在皮肤屏障受损、急性皮炎等皮肤问题的患者。在治疗中,医生会有选择地对这两类患者使用医用敷料,达到辅助修复、(对急性皮炎等)冷敷舒缓的作用。”上海市皮肤病医院、同济大学附属皮肤病医院皮肤与化妆品研究室副主任邹颖教授向记者介绍。
而配方师彭冠杰表示,在医美诊所中,医美术后修复贴主要面向轻医美术后患者:“轻医美手术后,面部皮肤有一定轻微损伤,医用敷料可以为皮肤提供湿润、安全的环境,避免损伤状态的皮肤接触外界污染,降低术后感染风险,有助于皮肤的修复。”
根据国家药监局发布的《外科纱布敷料通用要求》定义,医用敷料主要用于清洁覆盖创面、吸收体内渗出液、为创面提供愈合环境,部分医用敷料还可用于手术过程中支撑器官或组织。
而据《化妆监督管理条例》定义,化妆品是指以涂擦、喷洒或者其他类似方法,施用于皮肤、毛发、指甲、口唇等人体表面,以清洁、保护、美化、修饰为目的的日用化学工业产品。
2)成分与膜布
医疗器械不要求全成分备案,因此在国家药监局官网上能够查询到的信息有限。从披露的信息来看,医用敷料的成分较为基础,配方也较为简单。
邹颖教授表示,医用敷料含有的主要是一些常用的保湿成分,比如透明质酸、类人胶原蛋白,不像化妆品会有很多品类的划分,根据具体宣称可以添加各种各样的成分,医用敷料还是不一样的。
此外,在膜布上,医用敷料与面膜之间也会有一定不同。彭冠杰表示,医用敷料在膜布选择上更注重安全性,而面膜则更侧重于体验感。
3)生产标准
据国家药监局发布的《医疗器械生产质量管理规范附录无菌医疗器械》内容显示,与人体损伤表面和黏膜接触的无菌医疗器械或单包装出厂的配件,其末道清洁处理、组装、初包装、封口的生产区域和不经清洁处理的零部件的加工生产区域应当不低于30万级洁净度级别。
据《化妆品生产企业卫生规范(2007年版)》规定,生产眼部用护肤类、婴儿和儿童用护肤类化妆品的半成品储存间、灌装间、清洁容器储存间应达到30万级洁净要求;其它护肤类化妆品的半成品储存间、灌装间、清洁容器储存间宜达到30万级洁净要求。(注:30万级洁净度级别主要标准:车间换气次数≥10次/小时,30万级净化每立方米(升)空气中≥0.5μm尘粒数为≤35*100000(1500),30万级净化每立方米(升)空气中≥5μm尘粒数为≤60000,微生物最大允许数量为30cfu/皿)
对于化妆品生产和医疗器械生产来说,30万级都只是基础标准,企业可以以更高的标准来自主制定生产规范。
4)安全性、有效性评价
医用敷料和面膜在产品安全性和有效性的评价形式上也存在一些不同。医用敷料的安全性及有效性评价通过临床评价进行,《医疗器械临床评价指导原则》规定了三种临床评价方式:
①列入《免于进行临床试验的医疗器械目录》产品的临床评价:申报与目录所述产品的对比资料及等同性说明;
②通过同品种医疗器械的医疗器械临床试验或者临床使用获得的数据进行分析评价;
③通过临床试验进行临床评价。
而化妆品的安全性和有效性评价主要通过微生物检验、毒理学安全性实验、人体功效评价试验等来进行。
5)分类管理
与面膜不同,我国医疗器械在监管上实行分类管理,按风险程度由低到高,依次分为第一类(I类)、第二类(II类)和第三类(III类),医用敷料可以任意一类中注册备案。

技术壁垒只是一张生产许可证?
从上文的对比情况来看,医用敷料在生产标准和安全性上的硬性要求要高于面膜。而在监管体系上,面膜归属于化妆品,由国家药监局统一管理,相较于可在省、市药监局进行注册、备案的医疗器械,一定程度上会更严格一些。
在成分和配方上,医用敷料以玻尿酸、胶原蛋白等低功效性、高安全性的成分为主,配方精简、原料成本较低。在最终的产品价格上,以敷尔佳为例,其天猫旗舰店中的一款白膜医用敷料的价格为118元/5片,单片价23.6元,而其在招股书中所示的同行业对比公司珀莱雅的神经酰胺面膜价格为99元/20片,单片价4.95元,两者差价超过五倍。
那么,在医用敷料与面膜的成倍差价之间,有什么技术壁垒吗?
邹颖教授表示:“其实如果企业想申请二类器械的生产许可证,只要生产条件符合国家相应的管理条例、法律法规的要求,就是可以达到的。但是在工艺、材料、制剂上,不同的品牌和产品之间会存在一定的差异。”
而彭冠杰则表示:“从实际生产成本上,医用敷料的生产成本真的没有比面膜高,甚至一些好的面膜,成本比医用敷料还贵不少。医用敷料的技术壁垒,更多在于生产许可证的资质以及符合要求的生产环境工厂。但其实,在前几年,很多化妆品生产工厂的车间,也通过中介申请了“械字号”的生产许可证,车间环境基本上也是符合‘械字号’要求的。”
据美商社2019年《“医美面膜”火爆背后——是风口还是泡沫?》一文报道,化妆品工厂申请械字号生产资质的成功率不低,办理备案只要6个月左右,费用在4-6万不等。
医用敷料领域目前存在的一些问题
1)有企业化身总经销,合法化医用敷料生产
此外,美商社调查发现,医用敷料在生产环节存在大量的灰色空间,特别是自有品牌产品。品牌方只需注册10类医疗器械类商标品牌,设计完成后交给代工厂完成贴牌制作即可,因为一般品牌都不具备械字批文资格,找企业加工不能授权委托,否则属于违法操作,而客户(品牌方)以委托方作为总经销身份来销售,就能“合法化”。同样的面膜,在去代工厂镀了“械字号”的金后,售价翻了几番。
虽然已经时隔两年,但这不禁让人联想到日前在创业板递交上市申请的敷尔佳。据其招股书透露,在哈尔滨敷尔佳科技发展有限公司(公司前身,简称“敷尔佳有限”)设立之初,是作为“敷尔佳”产品的全国总代理与哈三联(哈尔滨三联药业股份有限公司)合作。其中,哈三联负责产品的独家生产,敷尔佳有限负责产品的独家销售、推广及品牌运营维护等。
据其招股书显示,在2021年2月前,敷尔佳有限自身并不具备医疗器械生产许可证。2018-2020年,敷尔佳有限几乎没有自产产品,主营业务产品均来自外部采购,企业运营重度依赖哈三联。直到2021年2月,敷尔佳有限换股收购哈尔滨北星药业有限公司(哈三联全资子公司),才由此拥有自主生产的能力。
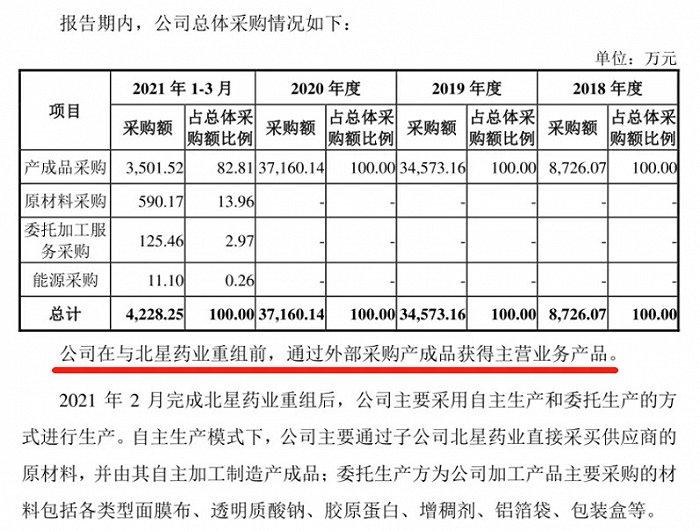
截图自敷尔佳有限招股书
曾一度被称为“医用敷料第一股”的敷尔佳有限,实则独立研发能力存疑。其招股书显示,截止至2021年3月31日,公司研发人员仅2名,占总员工数的0.69%。2018年-2021年第一季度,公司的研发投入分别为30.78万元、60.39万元、147.97万元和13.2万元,占营收比例分别为0.08%、0.04%、0.09%、0.04%,均不足千分之一。

截图自敷尔佳有限招股书
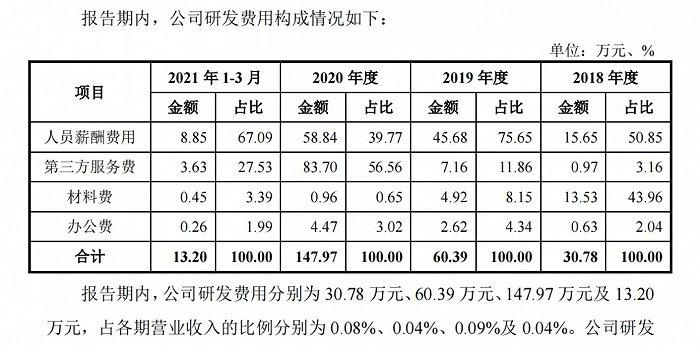
截图自敷尔佳有限招股书
2)“身在械,心在妆”
此前,曾有媒体将医疗器械定义为处于药品和化妆品之间的品类,但实际上医疗器械应该是独立于药品和化妆品的。医疗器械本身对人体并不具备药理学、免疫学或代谢等效用,和药品存在着本质的不同。药品、医疗器械、化妆品三者之间的边界,都应该被明确划分。但医疗器械(特别是医用敷料)与化妆品的分界线,从市场端部分品牌的宣传情况来看,仍然是不够明晰的。
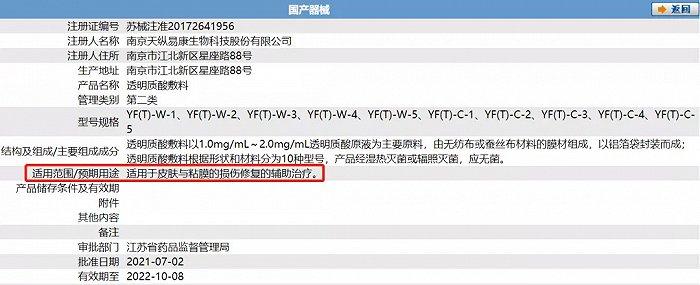
存在包装模仿化妆品、产品备案/注册信息与宣传不符、宣传夸大失实等问题的医疗器械,在电商平台比比皆是。如益肤的透明质酸敷料(实为第二类医疗器械),其天猫平台的详情页上显示产品具有对皮炎、湿疹、痤疮等辅助修复的作用,但其注册的适用范围/预期用途是适用于皮肤与黏膜的损伤修复的辅助治疗,脱离了预期用途的范围。
截图自国家药监局官网
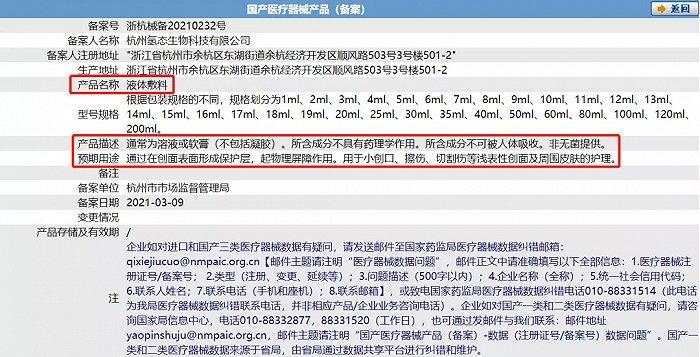
除贴片式医用敷料外,液体辅料也存在类似问题,如卫时丽液体敷料(实为第一类医疗器械)。该液体敷料在天猫平台的产品信息显示其具有保湿滋润,以小分子渗透修复受损细胞的作用。

截图自产品详情页
但其备案信息中的产品描述则显示,所含成分不可被人体吸收。预期用途为通过在创面表面形成保护层,起物理屏障作用。而在电商平台,该产品则公然宣称具有护肤品甚至药品才有的清洁力、修复力。广告宣传严重脱离产品预期用途。
截图自国家药监局官网
此外,芙清、帕兰蒂尔、蓝润、纪复康等品牌也存在相关问题。
对于医用敷料大量出现在电商平台,甚至被消费者当做面膜来日常使用的现象,彭冠杰表示:“医用敷料本质上是不应该出现大众电商平台的,它应该是专业医美渠道门诊专门给术后患者配套使用的。某些厂商利用了消费者对‘医美、医疗器械等’的信任感,误以为会比面膜更好更有效,其实不然。医用敷料与面膜,虽然外观、使用方法等都很像,但是设计的初衷和针对问题完全不同,两者不能混为一谈。”
邹颖教授也表示:“有一些企业确实在宣传上过度了,普通消费者并不需要常规地去使用这样的医用敷料,因为毕竟不是化妆品,所以还是要在医生的指导下、一些特定的场景里去使用,而不应该把敷料和化妆品的界限模糊掉、偷换概念,这样是不合适的。”
医用敷料市场确实存在一些乱象,特别是2018年-2019年医用敷料刚站上风口时尤甚。不过,自2020年1月起,国家药监局发布《化妆品科普:警惕面膜消费陷阱》后,对于医用敷料的监管逐渐收严。
2021年8月,国家药监局发布的《第一类医疗器械产品目录》修订草案(征求意见稿)对第一类医疗器械产品禁止添加成分名录做出了规定,神经酰胺、胶原蛋白、多肽、透明质酸、玫瑰提取物、洋甘菊提取物等化妆品常见成分都拟禁止添加在第一类医疗器械中。若此次征求意见稿能够落地,对于第一类医疗器械和化妆品将会有一定的区隔作用。
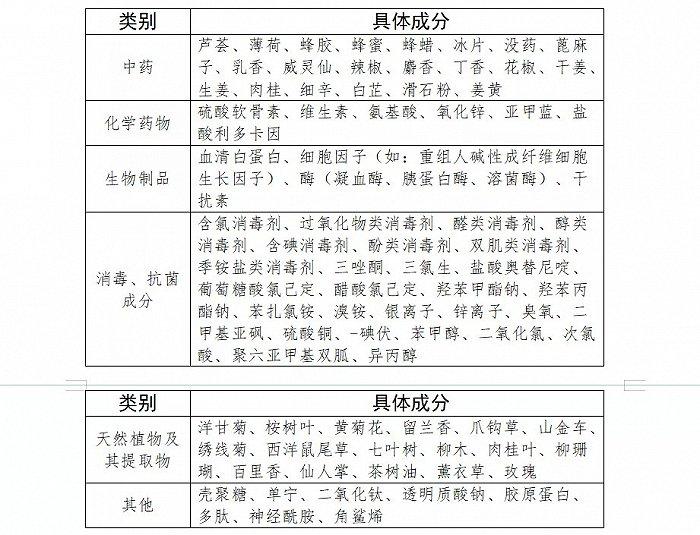
截图自《第一类医疗器械产品目录》修订草案(征求意见稿)
以目前医用敷料市场的热度,仍有不少企业试图通过械字号“降维打击”化妆品。而部分消费者在各路非专业美妆博主的不科学传播影响下,形成了医用敷料比普通面膜“高级”的认知。
但综上所述,我们可以看到,实际上从用途到原理,医用敷料都不应该和化妆品放在一起比较,至于哪个更专业、更安全也就无从谈起了。“械字号”只是产品的注册、备案号,不应该成为品牌吸引消费者的“金字招牌”,更不应该成为讲述其科研实力的“佐证”。


